
L’aspartame est un édulcorant de synthèse au pouvoir sucrant 150 à 200 fois supérieur à celui du sucre. Il est utilisé pour donner une saveur sucrée sans apporter de calories.
On le retrouve dans plus de 2 500 produits en Europe, et environ 6 000 dans le monde, principalement dans les produits dits « light », « zéro » ou « allégés en sucre »1,2.
Il représente un enjeu économique majeur pour les industriels puisqu’il est extrêmement rentable : sa puissance sucrante permet d’en utiliser des quantités infimes, pour un coût environ dix fois inférieur à celui du sucre3. Les économies réalisées par les fabricants sont considérables, mais rarement répercutées sur les prix de vente. Les boissons classiques et leur version sans sucre sont ainsi souvent vendues au même prix, voire plus cher dans certains cas, ce qui permet de maximiser les marges.
Mais la sécurité de l’aspartame est aujourd’hui largement remise en question. De nombreux scientifiques et journalistes d’investigation dénoncent des effets toxiques minimisés par des études biaisées, ainsi que des conflits d’intérêts entre industriels et autorités sanitaires ayant conduit à son autorisation.
Dans cet article, nous décryptons les zones d’ombre qui entourent l’aspartame et nous faisons le point sur ce que dit réellement la science.
Une mise sur le marché très controversée
1965 : naissance d’un édulcorant sous influence
L’aspartame est découvert par hasard en 1965 par un chimiste de l’entreprise pharmaceutique américaine Searle. Ce chimiste prénommé James Schlatter travaille sur un médicament contre les ulcères, lorsqu’il synthétise une nouvelle molécule. En goûtant accidentellement le composé sur ses doigts, il remarque son goût extrêmement sucré4.
Son pouvoir sucrant, bien supérieur à celui du sucre, suscite rapidement l’intérêt de la société, qui engage alors une procédure d’autorisation auprès de la FDA (Agence américaine des produits alimentaires) pour permettre son utilisation dans des produits alimentaires courants.
Searle finance alors plusieurs tests en laboratoire pour évaluer la toxicité de l’aspartame et transmet les résultats à la FDA en 1973. Dans la foulée, en 1974, la FDA approuve sa mise sur le marché dans les aliments secs et les chewing-gums. Cette décision se base sur une première lecture sommaire des études de toxicité fournies par Searle et sur l’hypothèse simpliste selon laquelle l’aspartame serait inoffensif puisqu’il se dégrade dans l’organisme en deux composés naturellement présents dans le corps humain5.
Cette autorisation suscite immédiatement des critiques, notamment de la part du neuroscientifique John Olney, qui alerte sur le risque de lésions et de tumeurs cérébrales6. Dès l’année suivante, en 1975, la mise sur le marché de l’aspartame est suspendue pour permettre une investigation plus approfondie de la part des scientifiques de la FDA7.
Après 2 ans de travail, ces derniers soulèvent de graves problèmes. Ils pointent de nombreuses négligences et irrégularités dans les études menées sur des rats et des souris : symptômes non signalés ayant nécessité des antibiotiques, retrait de tumeurs avant dissection sans mention dans les rapports, ou encore impossibilité d’examiner certains organes trop dégradés8,9. Au total, 52 anomalies majeures sont relevées dans seulement trois études parmi les 15 études toxicologiques fournies par Searle10,11. Face à la gravité des faits, le chef du service juridique de la FDA engage des poursuites contre Searle pour « rétention de données et fausse déclaration »12,13. La FDA mandate également un comité de scientifiques extérieurs à l’agence pour statuer sur la sécurité de l’aspartame. C’est la première fois que la FDA recourt à ce procédé, appelé Public Board of Inquiry, pour trancher une question de sécurité sanitaire14. En 1980, après plusieurs mois d’investigation, le comité conclut à l’unanimité contre la réautorisation de l’aspartame15.
L’élection de Ronald Reagan à la présidence des États-Unis en 1980 marque cependant un tournant important dans l’histoire de l’aspartame. Donald Rumsfeld, alors PDG de Searle, est loin d’être un inconnu à Washington : il a déjà occupé des postes de haut niveau dans l’administration, notamment celui d’ambassadeur des États-Unis auprès de l’OTAN et de chef de cabinet à la Maison Blanche sous Gerald Ford9.

Après avoir quitté la politique pour rejoindre Searle, il s’implique activement dans la campagne présidentielle de Ronald Reagan. Avec la victoire de ce dernier, Rumsfeld rejoint à nouveau le gouvernement en intégrant le Comité consultatif intérimaire sur la politique étrangère. Il joue alors un rôle clé dans la nomination du nouveau président de la FDA16. Arthur Hayes, un proche de Rumsfeld sans aucune expérience dans le domaine des additifs alimentaires, est ainsi désigné à la tête de l’agence. Moins de deux mois après sa prise de fonction, en juillet 1981, Hayes autorise à nouveau l’aspartame17, d’abord pour une utilisation dans les aliments secs, puis dans les boissons, avant de l’étendre à tous les produits alimentaires en 1996. Il déclare : « Je ne suis pas prêt à dire qu’il n’y a aucun risque lié à l’aspartame, mais je pense qu’il a été démontré qu’il n’y avait pas de risque significatif. »18

Cette décision va à l’encontre des conclusions des toxicologues de la FDA et des experts indépendants du Public Board of Inquiry19. Plus surprenant encore, elle contredit aussi la position du principal lobby américain des boissons, la National Soft Drink Association. L’organisation s’était opposée à l’utilisation de l’aspartame dans les sodas, jugeant que la substance pouvait se dégrader en composés toxiques lors du stockage. En 1983, elle déclare d’ailleurs : « Searle n’a pas apporté la certitude nécessaire pour garantir que l’aspartame et ses produits de dégradation sont sûrs dans les boissons gazeuses. »20
Pour légitimer la réautorisation de l’aspartame aux États-Unis, deux nouvelles études sont présentées21,22. Toutes deux sont menées et financées par Ajinomoto, l’un des principaux fabricants mondiaux… d’aspartame ! Ces travaux, portant sur les risques de cancer et sur les autres effets toxiques à long terme de l’aspartame, concluent à une absence de toxicité. Mais comme les études précédentes menées par Searle, ces travaux d’Ajinomoto sont loin de faire l’unanimité. D’abord, ils n’ont jamais été soumis à une relecture par des pairs — une étape pourtant fondamentale pour garantir la validité scientifique d’une étude23. Ensuite, leur méthodologie ne respecte pas les standards toxicologiques en vigueur à l’époque24,25.
Par ailleurs, l’étude sur le cancer menée par Ajinomoto en 198121, utilisée pour justifier la réautorisation, se limite exclusivement aux tumeurs cérébrales, ignorant ainsi la possibilité que d’autres organes puissent également être affectés par un risque de cancer. Cette approche avait pourtant été jugée insuffisante d’un point de vue toxicologique par les scientifiques internes de la FDA de l’époque26 pour justifier une autorisation de mise sur le marché.
Des liens troublants entre la FDA et les fabricants d’aspartame
Au-delà de reposer sur des études contestées, l’approbation de l’aspartame soulève aussi la question des conflits d’intérêts. Et pour cause : six hauts responsables de la FDA impliqués dans l’approbation finale de l’édulcorant en 1981 ont, peu après, rejoint des entreprises liées à la production… d’aspartame27 !
Autre élément troublant : Samuel Skinner, le procureur fédéral chargé de mener l’action judiciaire de la FDA contre Searle pour les irrégularités dans ses études, démissionne le 1er juillet 1977. Or, il ne restait que quelques mois pour agir, jusqu’en décembre 1977, avant que les délais de prescription ne rendent toute action impossible. Peu après, Skinner rejoint le cabinet d’avocats… chargé de défendre Searle dans cette affaire ! Son remplaçant, William Conlon, arrivé trop tard, n’a pas eu le temps de reprendre le dossier. Résultat : les poursuites sont abandonnées et Searle échappe définitivement à toute sanction. Étrangement, Conlon finit par rejoindre le même cabinet d’avocat chargé de défendre Searle moins d’un an plus tard12,28.
Autre illustration des conflits d’intérêts, une enquête révèle qu’Arthur Hayes, nommé président de la FDA en 1981, a accepté plusieurs avantages offerts par des industriels29, notamment la mise à disposition d’un jet privé appartenant à General Food Corporation, un distributeur d’aspartame18. Ces révélations auraient contribué à sa démission en 198330. Peu après, il rejoint Burson-Marsteller, l’agence de relations publiques de Searle, en tant que consultant scientifique senior13.
Europe : une expertise de l’EFSA qui soulève également des doutes
Malgré les nombreuses controverses aux États-Unis, l’élan est lancé. D’autres pays commencent à autoriser l’aspartame dans les produits du quotidien en s’appuyant sur l’approbation américaine, et sans exiger d’études complémentaires : le Canada en 198131, l’Australie en 198632, puis l’Union européenne en 199433.
Une réévaluation en 2013 largement critiquée
En 2013, l’Autorité européenne de sécurité des aliments (EFSA) réévalue la sécurité de l’aspartame pour son utilisation en Union Européenne, et conclut à l’absence de danger34,35. Mais cet avis suscite à son tour des critiques. En 2019, Erik Millstone et Elizabeth Dawson, deux chercheurs de l’University of Sussex au Royaume-Uni, publient une étude qui remet en cause cette évaluation36. Ils alertent sur la méthodologie de sélection des études toxicologiques par l’EFSA. En effet, ils indiquent que chacune des 73 études montrant des effets nocifs de l’aspartame sur la santé ont été écartées sans justification solide. A l’inverse, 43 des 62 études ne montrant pas ou peu d’impact de l’aspartame ont été prises en compte dans l’évaluation, soit plus des trois quarts. Or, certaines des études écartées étaient jugées par les deux experts comme « plus robustes et plus pertinentes » que celles retenues. Autre problème : parmi les études retenues, beaucoup étaient financées par les industriels et certaines avaient même été jugées « sans valeur », « frauduleuses » voire même de « désastre » par d’anciens toxicologues de la FDA37.
Or, s’appuyer sur des études financées par les industriels peut introduire des biais dans les résultats. Ce sont les conclusions de deux revues scientifiques publiées en 201638 et 201739 : les études financées par l’industrie alimentaire sont plus susceptibles de conclure à l’absence d’effets négatifs des édulcorants (notamment sur la prise de poids), par rapport aux études menées de manière indépendante.
Les études Ramazzini : des travaux de référence pourtant écartés par l’EFSA
L’EFSA a notamment écarté de sa réévaluation plusieurs études majeures40,41,42 sur les risques de cancer menées par l’Institut Ramazzini, un centre de recherche qui bénéficie pourtant d’une reconnaissance internationale en cancérologie43. L’EFSA a justifié cette décision par le fait que ces travaux ne respectaient pas les protocoles expérimentaux standards. Pourtant, ces travaux allaient bien au-delà des exigences habituelles : l’étude portait sur 1 400 rats (contre 400 dans les protocoles classiques), testait 6 niveaux de dose (au lieu de 3 habituellement), et laissait les animaux vivre jusqu’à leur mort naturelle afin de détecter d’éventuels effets cancérigènes tardifs, alors que les protocoles standard prévoient l’enthanasie des rongeurs au bout de deux ans44.
La critique principale de l’EFSA portait sur cette longévité inhabituelle des rongeurs : selon l’agence, les infections pulmonaires observées chez des animaux âgés rendaient « l’interprétation des résultats difficile ». L’EFSA suggérait ainsi que les tumeurs pouvaient être dues aux infections pulmonaires et non pas à la consommation d’aspartame34,45.
Or, selon les chercheurs de l’institut Ramazzini, ces infections font partie du « processus naturel de vieillissement de ces animaux »46. Surtout, elles ont également été constatées dans le groupe témoin, non exposé à l’aspartame, ce qui exclut leur implication dans le développement des tumeurs. La présence d’un groupe contrôle permet précisément d’écarter ce type de biais, en garantissant une comparaison rigoureuse.

La qualité des travaux de l’institut Ramazzini sur l’aspartame a ensuite été reconnue à plusieurs reprises. Un avis publié en 2008 par trois scientifiques américains, spécialistes des méthodologies expérimentales permettant d’évaluer la cancérogénicité des substances, souligne que le fait de prolonger la vie des animaux permet de « renforcer la valeur et la validité des résultats »47. Par ailleurs, comme nous l’a expliqué le chercheur Erik Millstone au cours d’un entretien, « les études de l’Institut Ramazzini étaient plus approfondies, fiables et pertinentes pour l’exposition humaine que celles réalisées selon les protocoles conventionnels ».
En 2021, l’institut Ramazzini a publié une nouvelle étude confirmant que les tumeurs observées chez les rongeurs dans ses premières études étaient bien liées à la consommation d’aspartame, et non aux infections pulmonaires qui apparaissent naturellement en fin de vie48. En 2023, la principale étude controversée a été ré-analysée par de nouveaux chercheurs de l’Institut Ramazzini et les conclusions sont restées inchangées49.
Enfin, le Centre international de recherche sur le cancer (CIRC) – une référence mondiale en matière de recherche sur le cancer – a confirmé la solidité de la méthodologie de l’Institut Ramazzini en 2024. Il a ainsi affirmé que l’extension de la durée de vie des rats était considérée comme l’une des principales forces de cette étude. Il a également souligné que la pureté de l’aspartame avait été correctement analysée. À l’inverse, le CIRC a jugé les travaux de Searle et Ajinomoto limités par l’absence d’informations sur la pureté et par le manque de détails en histopathologie50.
En refusant d’intégrer les données de l’Institut Ramazzini, l’EFSA a écarté certaines des preuves les plus solides disponibles sur les risques de cancer, soulevant ainsi des interrogations sur son impartialité. L’Institut Ramazzini a par la suite révélé en 2021 avoir subi de fortes pressions après ses publications sur l’aspartame. Les chercheurs à l’origine de ces travaux ont vu leur crédibilité attaquée et leurs recherches tournées en dérision par l’industrie agroalimentaire51,52,53, ce qui a conduit à une réduction significative de leurs financements54.
Le Center for Science in the Public Interest (CSPI), une ONG américaine reconnue pour son action en faveur de la santé publique, avait également dénoncé ces attaques contre l’Institut Ramazzini en 201355. L’organisation rappelle que les travaux de l’institut apportent « des preuves irréfutables que l’aspartame est cancérigène chez les animaux ».
L’EFSA également suspectée de conflits d’intérêt
Dans leur étude de 201936 sur la réévaluation de l’aspartame par l’EFSA, les chercheurs de l’Université de Sussex suggèrent que l’agence aurait été influencée par des conflits d’intérêt d’ordre commercial. Selon eux, cela pourrait expliquer pourquoi certaines études pourtant solides ont été écartées de la réévaluation menée par l’EFSA 2013.
Cette hypothèse rejoint les constats de l’ONG Foodwatch. Dans un rapport sur l’aspartame publié en 202556, l’organisation indique que, parmi les 62 études jugées fiables par l’EFSA, 45 présentent des conflits d’intérêts : elles sont soit directement financées par les fabricants d’aspartame, soit rédigées par des personnes collaborant en parallèle avec l’industrie liée à cet édulcorant.
L’analyse publiée par le Réseau Environnement Santé en 201357 va encore plus loin et révèle que 6 des 19 experts de l’EFSA ayant participé à la réévaluation de l’aspartame entretenaient des liens étroits avec l’industrie, notamment avec Ajinomoto, principal fabricant mondial d’aspartame, ou encore avec Coca-Cola, dont les boissons « light » et « zéro » reposent largement sur cet édulcorant. Plus préoccupant, cette analyse révèle qu’une partie du rapport de l’EFSA de 2013 est en réalité un copier-coller d’une publication de 2007 financée par Ajinomoto51. Sur les 96 lignes du rapport de l’EFSA consacrées aux risques neurologiques liés à l’aspartame, 60 sont identiques ou très proches du texte de la publication financée par Ajinomoto. Le Réseau Environnement Santé conclut dans son rapport que la réévaluation de l’EFSA en 2013 présente de graves manquements aux principes essentiels de la déontologie scientifique.
L’EFSA semble également avoir cherché à minimiser, voire à dissimuler, certains liens entre ses membres et l’industrie. C’est ce que révèle la journaliste d’investigation Marie-Monique Robin dans son documentaire Notre poison quotidien58, diffusé en 2011 sur Arte. Elle y montre que l’agence aurait modifié a posteriori une déclaration officielle de conflits d’intérêts. Le cas concerne Dominique Parent-Massin, membre du groupe de travail chargé d’évaluer l’aspartame. Dans sa fiche initiale, cette experte de l’EFSA indiquait avoir travaillé comme consultante pour Ajinomoto et pour Coca-Cola — deux entreprises directement concernées par l’édulcorant. Or, ces mentions auraient disparu de la fiche après que la journaliste a interviewé des membres du personnel de l’EFSA dans le cadre de son enquête sur l’aspartame. Cette modification efface ainsi toute trace d’un lien direct entre l’experte de l’EFSA et deux entreprises ayant un intérêt commercial majeur dans l’aspartame, soulevant un problème fondamental de transparence et d’indépendance.
Ces révélations vont dans le même sens que celles de l’ONG Corporate Europe Observatory. Dans un rapport publié en 201159, l’organisation explique que quatre membres du panel de l’EFSA chargé d’évaluer les additifs alimentaires n’avaient pas déclaré leurs collaborations actuelles et passées avec l’International Life Sciences Institute (ILSI Europe). Sous couvert d’être une organisation scientifique indépendante à but non lucratif, l’ILSI défend farouchement les intérêts de l’industrie alimentaire60. Elle a été fondée par un ancien vice-président de Coca-Cola, financée pendant des décennies par des entreprises comme Coca-Cola (jusqu’en 2021) et Mars (jusqu’en 2018), et compte aujourd’hui parmi ses membres Pepsi et Ajinomoto. Le rapport de l’ONG Corporate Europe Observatory conclut qu’il est urgent de mettre en place des règles plus strictes sur les conflits d’intérêts et de réformer en profondeur la manière dont l’EFSA élabore ses avis scientifiques.
Par ailleurs, le Parlement européen a vivement remis en question l’indépendance de l’EFSA dans un rapport publié en 201461,62, appelant à une véritable politique de transparence et de prévention des conflits d’intérêts. En réponse, l’agence a pris plusieurs mesures : en 201463, elle a instauré des règles pour prévenir les conflits d’intérêts parmi ses membres. En 201564, elle a revu sa méthodologie de sélection des études afin d’éviter que conclusions soient arbitrairement écartées. Enfin, en 201965, un règlement européen a été adopté pour renforcer la transparence de l’EFSA. Cependant, malgré ces progrès, l’avis de 2013 sur l’aspartame n’a toujours pas été actualisé.
Face à toutes ces révélations, plusieurs scientifiques appellent aujourd’hui à une réévaluation indépendante de l’aspartame au niveau européen36,48,66,67,68.
Des risques bien documentés
Cancer : un risque accru à partir d’une demi-canette par jour
En 2023, le Centre international de recherche sur le cancer (CIRC) a classé l’aspartame comme « cancérigène possible » (groupe 2B)69. Cette décision repose sur un vaste travail de synthèse réalisé par le CIRC, qui a passé en revue toutes les études publiées depuis 1974 sur le potentiel cancérogène de cet édulcorant. Dans un rapport de 471 pages70, le CIRC conclut que l’aspartame est un cancérigène possible pour l’être humain.
En complément des études animales, cette classification s’appuie également sur des données humaines, notamment issues de la prestigieuse cohorte française NutriNet-Santé de l’Institut national de la santé et de la recherche médicale (INSERM) de 202271. Cette étude de grande envergure suit les habitudes alimentaires de plus de 100 000 Français depuis 13 ans. Elle montre qu’une consommation régulière d’aspartame serait associée à une augmentation de 15 % du risque global de cancer, avec un risque encore plus marqué pour le cancer du sein, où l’augmentation atteint jusqu’à 22 %. Les personnes consommant de l’aspartame régulièrement, soit l’équivalent d’une demi canette de soda par jour, seraient plus susceptibles de développer ces cancers. C’est la première étude au monde à établir une association aussi précise et rigoureusement vérifiée entre l’exposition à l’aspartame et le risque de cancer. Ainsi, le CIRC la considère comme « l’étude la plus détaillée et de la plus haute qualité » sur l’exposition humaine à cet édulcorant.
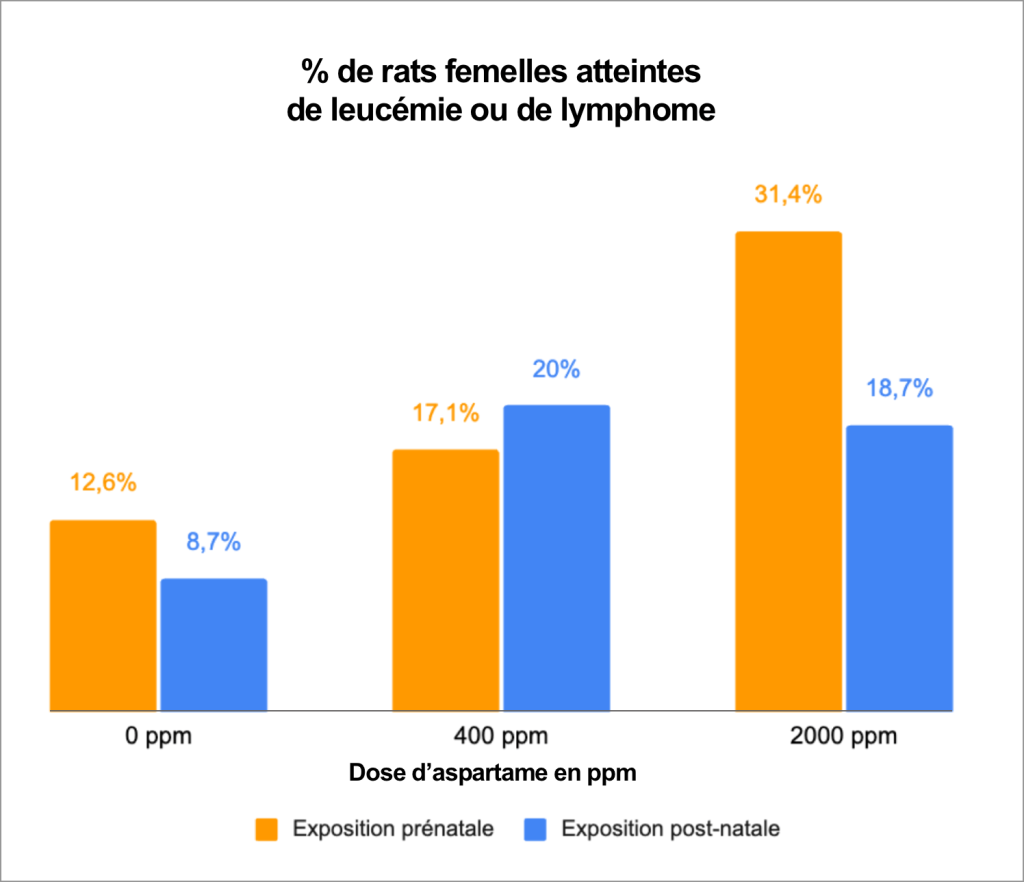
Une précédente étude épidémiologique menée par l’Université Harvard et publiée en 201272, ayant suivi plus de 120 000 Américains pendant plus de 22 ans, avait également identifié ces risques de cancer et mis en évidence une association statistiquement significative entre la consommation de boissons édulcorées à l’aspartame et une augmentation de 31 % du risque de lymphome non hodgkinien, ainsi que de 102 % du risque de myélome multiple.
Selon certains membres du groupe d’experts du CIRC, l’aspartame aurait même dû être classé dans la catégorie supérieure, en tant que « cancérigène probable » (groupe 2A). En effet, ils considéraient que l’Institut Ramazzini apportait des preuves suffisantes d’une cancérogénicité chez les animaux de laboratoire70. Les chercheurs de l’institut Ramazzini ont d’ailleurs contesté la manière dont leurs données ont été traitées par le CIRC. Selon eux, ce dernier a sous-évalué leurs résultats. Les chercheurs concluent que l’évaluation du CIRC sur l’aspartame pourrait « avoir été guidée par d’autres considérations que l’évaluation scientifique impartiale des données disponibles », suggérant ainsi la possibilité de conflits d’intérêts au sein du groupe de travail du CIRC73.
De nombreuses études menées sur des cellules humaines et animales ont identifié plusieurs mécanismes pouvant expliquer l’apparition de tumeurs. Selon le CIRC, le plus probable pour l’aspartame est le stress oxydatif. Lorsqu’il est digéré, l’aspartame se transforme en substances pouvant générer des radicaux libres : il s’agit de molécules instables qui, en trop grande quantité, peuvent oxyder – c’est-à-dire abîmer – les cellules. Avec le temps, ces dommages peuvent perturber le fonctionnement de nos cellules et augmenter le risque de cancer70.
Aujourd’hui, la suspicion de cancérogénicité de l’aspartame repose sur un ensemble de preuves issues de trois approches complémentaires :
- Tout d’abord, les études animales menées par l’Institut Ramazzini40,41,42, dont le protocole, plus exigeant que les standards habituels, a permis d’obtenir des résultats largement reconnus par la communauté scientifique.
- Ensuite, des études épidémiologiques menées chez l’homme, dont l’une — jugée par le CIRC comme la plus complète et rigoureuse sur le sujet71 — a mis en évidence une association significative entre consommation d’aspartame et augmentation du risque de cancers.
- Enfin, des recherches ayant identifié un mécanisme d’action cohérent expliquant l’apparition de tumeurs70.
La convergence de ces données, provenant de méthodes et disciplines différentes, forme un faisceau d’indices suffisant pour que le CIRC considère l’aspartame comme présentant un risque cancérogène possible chez l’humain.
Les quelques recherches ayant conclu à l’absence de risque cancérigène de l’aspartame ont, sans surprise, souvent été financées par l’industrie. De plus, elles présentent fréquemment des limites majeures. En effet, certaines reposent sur une méthodologie discutable, comme les études financées par Searle et Ajinomoto dans les années 198021,22. D’autres utilisent des souris génétiquement modifiées, un choix que le CIRC juge inadapté car ces animaux pourraient être insensibles à l’aspartame70. Enfin, certains travaux se limitent à un seul type de cancer très spécifique, ou bien reposent sur une période d’observation trop courte, ce qui empêche de détecter d’éventuels effets à long terme. Ainsi, la solidité scientifique de ces études reste bien inférieure à celle des études menées de façon indépendante et rigoureuse.
Un édulcorant qui pourrait favoriser le diabète
Comme d’autres édulcorants artificiels, l’aspartame est depuis plusieurs années soupçonné de favoriser, sur le long terme, l’apparition d’un diabète de type 2.
Cette maladie chronique correspond à un dérèglement progressif du mécanisme qui régule le glucose (taux de sucre) dans le sang. C’est la forme la plus répandue de diabète : elle touche plus de 460 millions de personnes dans le monde, soit près de 6 % de la population. Elle se développe le plus souvent à l’âge adulte, sous l’influence de nos habitudes de vie. Les principaux facteurs de risque sont bien connus aujourd’hui : sédentarité, alimentation déséquilibrée ou encore tabagisme74. Mais, depuis quelques années, les scientifiques soupçonnent également certains édulcorants – et notamment l’aspartame – de contribuer au développement de cette maladie.
Depuis 2008, douze études de cohorte reconnues solides par l’OMS75, montrent qu’une consommation régulière de boissons édulcorées pourrait augmenter le risque de développer un diabète de type 2. Par exemple, une étude française publiée en 201376, menée auprès de 66 000 femmes, révèle que les consommatrices régulières de boissons édulcorées présentent jusqu’à deux fois plus de risque de développer un diabète de type 2 que celles qui n’en consomment pas. De façon surprenante, dans certains scénarios, ce risque était comparable à celui observé chez les personnes consommant régulièrement des boissons sucrées classiques, pourtant connues pour favoriser le diabète. Des résultats similaires ont été observés dans d’autres études menées sur l’être humain, publiées en 200977 et 201478, ainsi que sur l’animal en 201779.
Trois mécanismes principaux sont envisagés pour expliquer ces résultats :
- Les édulcorants pourraient entretenir, voire renforcer, l’attrait pour le goût sucré, incitant à consommer davantage de produits sucrés80.
- Les édulcorants, notamment l’aspartame, pourraient provoquer des réactions physiologiques similaires à celles du sucre, en activant les récepteurs du goût sucré présents non seulement dans la langue, mais aussi dans l’intestin et le pancréas. Une étude américaine de 201081 a ainsi montré que la consommation d’aspartame entraînait une augmentation du taux d’insuline comparable à celui provoqué par la consommation de sucre trente minutes après l’ingestion du repas.
- Enfin, les édulcorants pourraient déséquilibrer le microbiote, entraînant une inflammation chronique qui favorise la résistance à l’insuline et augmente le risque de diabète de type 282.
En 2023, une étude issue de la cohorte française NutriNet-Santé83, saluée pour sa rigueur méthodologique, a apporté des résultats encore plus précis. Elle révèle qu’une consommation régulière d’une petite quantité d’aspartame pourrait augmenter de 48 à 63 % le risque de développer un diabète de type 2. Les auteurs concluent que ces édulcorants ne peuvent pas être considérés comme des substituts sûrs au sucre, même lorsqu’ils sont utilisés à faibles doses.
De nombreuses autres études ont également mis en évidence une association entre la consommation d’édulcorants et le diabète84. Une étude publiée en 2022 va même jusqu’à considérer que les édulcorants, et en particulier l’aspartame, pourraient « contribuer à la pandémie de diabète dans certains contextes »82.
Une augmentation du risque de maladies cardio-vasculaires
L’aspartame est également suspecté d’accroître le risque de maladies cardiovasculaires. Ces pathologies — infarctus, accidents vasculaires cérébraux (AVC), thromboses veineuses, embolies pulmonaires, etc. — affectent le cœur et les vaisseaux sanguins, et constituent la première cause de mortalité dans le monde85.
En avril 2022, l’Organisation mondiale de la santé (OMS) a publié un rapport sur les effets des édulcorants75, basé sur 280 études menées chez l’humain. Parmi elles, 56 portaient spécifiquement sur les maladies cardiovasculaires. Leur synthèse montre que les consommateurs réguliers d’édulcorants présentent un risque accru de 32 % de développer une maladie cardiovasculaire, et de 19 % en ce qui concerne les accidents vasculaires cérébraux (AVC). De plus, toujours selon l’OMS, la consommation régulière d’édulcorants favoriserait à long terme l’hypertension et le déséquilibre du cholestérol, deux facteurs de risque dans le déclenchement de complications cardiovasculaires.
Ces résultats vont dans le même sens que ceux de l’étude française NutriNet-Santé, publiée en septembre 202286, qui s’est penchée spécifiquement sur l’impact de l’aspartame sur la santé cardiovasculaire. Elle révèle que les consommateurs réguliers présentaient un risque d’AVC accru de 17 %, une estimation proche de celle avancée par l’OMS.
Face à ces résultats préoccupants, l’OMS a formulé l’année suivante, en 2023, une recommandation sans ambiguïté : ne pas consommer d’édulcorants à des fins de réduction d’apparition de maladies chroniques, notamment de maladies cardio-vasculaires87.
Une étude de 202588, utilisant un protocole récent d’analyse des liaisons chimiques, apporte des éléments d’explication à ces observations. Elle indique que l’aspartame pourrait interagir avec plusieurs protéines et récepteurs du cerveau, entraînant des interférences multiples qui favorisent l’hypertension et le risque d’AVC. Les chercheurs vont jusqu’à suggérer de potentielles incompatibilités entre une consommation quotidienne d’aspartame et la prise de certains médicaments destinés à faire baisser la pression artérielle.
Un impact délétère sur le microbiote
Le microbiote intestinal désigne l’ensemble des milliards de micro-organismes qui peuplent nos intestins et jouent un rôle clé dans notre santé89. Lorsqu’il se déséquilibre, il peut favoriser l’apparition de nombreuses maladies chroniques90,91,92,93 (voir notre article sur le microbiote).
En 2014, une étude publiée dans la prestigieuse revue Nature a été la première à mettre en évidence un effet négatif des édulcorants sur le microbiote de personnes en bonne santé94. Les chercheurs ont constaté une diminution de la diversité microbienne. Ce phénomène est susceptible, à long terme, de favoriser des troubles métaboliques comme la résistance à l’insuline, l’intolérance au glucose, ainsi que des pathologies chroniques déjà évoquées : cancers, diabète de type 2 et maladies cardiovasculaires.
En 2014, une étude s’est penchée spécifiquement sur l’aspartame95. Elle montre que, même à des doses courantes — équivalentes à deux canettes de soda par jour —, l’aspartame peut altérer durablement l’équilibre du microbiote intestinal.
D’autres travaux publiés en 202096 ont mis en évidence un phénomène aggravant : l’aspartame pourrait endommager l’épithélium intestinal, cette fine barrière de cellules qui nous protège des agents pathogènes. Sa détérioration favoriserait une inflammation chronique de l’intestin et affaiblirait le système immunitaire, augmentant ainsi le risque de développer des maladies chroniques.
Des recherches supplémentaires restent nécessaires pour mieux comprendre le lien entre édulcorants, microbiote et maladies chroniques. Mais cette hypothèse est aujourd’hui largement jugée plausible par la communauté scientifique97,98,99. Dans son rapport de 202275, l’OMS souligne d’ailleurs que certaines maladies chroniques pourraient être liées à une altération du microbiote intestinal provoquée par la consommation d’édulcorants.
Une suspicion de neurotoxicité
Les premiers signaux d’alerte sur la possible toxicité neurologique de l’aspartame remontent aux années 1970. À l’époque, le neuroscientifique John Olney avait observé que, même à des doses relativement faibles, l’édulcorant pouvait détruire les neurones de souriceaux dont le cerveau était encore en développement100,101. Depuis, ces inquiétudes ont refait surface à plusieurs reprises, alimentées par de nouvelles études.
En 2008, des chercheurs ont montré que l’aspartame se décompose dans l’organisme en trois substances102 : la phénylalanine, l’acide aspartique et le méthanol. Or, toutes sont connues pour interagir avec le système nerveux. Elles peuvent ainsi perturber l’action des neurotransmetteurs, comme la dopamine ou la sérotonine. Elles pourraient aussi provoquer des maux de tête, troubles de la mémoire et du sommeil, variations d’humeur, stress ou dépression4,103. Enfin, elles peuvent générer un stress oxydatif dans le cerveau, endommageant les neurones et favorisant leur dégénérescence104.
Deux études de 2023105 et 2024106 ont montré que ces effets étaient observés chez la souris à des très faibles doses d’aspartame, comparables à une consommation courante chez l’humain. Ces effets sont apparus en seulement quatre semaines et, plus inquiétant encore, ont été transmis à la descendance des souris exposées, suggérant que les effets indésirables de l’aspartame sur le cerveau pourraient se transmettre aux générations suivantes.
L’OMS indique quant à elle que, chez l’humain, les résultats restent contrastés : certaines études mettent en évidence un lien entre l’aspartame et des troubles cognitifs — notamment un risque accru de maladie d’Alzheimer —, tandis que d’autres ne relèvent aucune association75. Des recherches plus approfondies sont donc nécessaires pour déterminer si les effets observés chez l’animal se produisent aussi chez l’être humain.
Une DJA devenue obsolète et insuffisante
La DJA (dose journalière admissible) correspond à la quantité maximale d’une substance qu’une personne peut consommer chaque jour, toute sa vie, sans risque pour la santé. Elle est calculée en fonction du poids : on l’exprime en milligrammes (mg) de substance par kilogramme (kg) de poids corporel107.
Cette limite est fixée par des agences d’évaluation des risques, comme l’EFSA pour l’Union européenne ou la FDA pour les États-Unis. Pour cela, ils repèrent la dose la plus faible qui provoque un effet dans des études sur les animaux, puis appliquent une marge de sécurité (généralement un facteur 100) pour déterminer une valeur supposée sans effet chez l’humain. Cette méthode, bien qu’utile, présente toutefois certaines limites.
Un seuil défini par les fabricants dans les années 70
La DJA actuelle de l’aspartame repose sur des études anciennes et controversées. En 1980, le JECFA, qui est le comité chargé de fixer les DJA au niveau mondial, a fixé ce seuil à 40 mg/kg de poids corporel/jour108. Cette décision a été largement influencée par la FDA, dont plusieurs scientifiques siégeaient également au JECFA109. Par ailleurs, la FDA était la seule à détenir, à l’époque, l’ensemble des données toxicologiques disponibles, mais elle n’a pas permis au JECFA de prendre pleinement en compte les fraudes et faiblesses méthodologiques des études en question. En effet, ces limites ne sont aucunement mentionnées dans les rapports du JECFA.
Pour définir cette DJA, le JECFA s’est appuyé sur des travaux financés par les fabricants Ajinomoto et Searle. L’étude clé retenue pour fixer la DJA est celle réalisée sur les rats en 1981 par Ajinomoto22, une étude très controversée dont la méthodologie était déjà très contestée à l’époque par de nombreux scientifiques12,110.
En 1983, la FDA adopte une DJA encore plus souple de 50 mg/kg/jour, sans appuyer cette décision sur de nouvelles études111.
En Europe, l’EFSA fixe également en 1984 la DJA à 40 mg/kg/jour, au moment de la mise sur le marché de l’aspartame112. L’EFSA fait pour cela confiance aux évaluations de la FDA et du JECFA, sans demander d’études supplémentaires58. L’EFSA indique dans son rapport avoir évalué une grande quantité de données sans préciser ni les études en question ni les résultats de ces études. Plus tard, lors d’une audition au Parlement européen en 2011, l’EFSA avouera que le comité scientifique de l’époque n’avait, en réalité, jamais disposé des études initiales de Searle et Ajinomoto et avait autorisé l’aspartame dans toute l’Union européenne les yeux fermés112.
Un statu quo maintenu en 2013 sans justification
En 201334, l’EFSA a réévalué l’aspartame et a maintenu la valeur de la DJA fixée en 1984 : 40 mg/kg de poids corporel/jour113. Selon les estimations de l’OMS, cela équivaut à une consommation quotidienne de 9 à 14 canettes de soda114,115, une quantité qui peut sembler extrême et donc rassurante pour tout consommateur ordinaire de sodas.
Cependant, comme mentionné précédemment, cette réévaluation est entachée de critiques et soulève un problème majeur : la sélection biaisée des études. En effet, l’EFSA a eu tendance à privilégier les travaux les plus rassurants sur l’aspartame, et à écarter les études qui signalaient des risques, y compris celles présentant une méthodologie jugée plus robuste que celle des travaux retenus36,57.
L’agence indique se baser sur l’étude très contestée de 1981 financée par le fabricant d’aspartame Ajinomoto22. Son rapport ne mentionne à aucun moment les limites méthodologiques majeures de cette étude. L’une des principales limites de cette étude concerne l’absence de données sur la pureté de l’aspartame70 : aujourd’hui, rien ne permet d’affirmer avec certitude que la substance administrée aux rats de l’étude était bien de l’aspartame pur. Pour balayer cette réserve, l’EFSA indique simplement que, pour l’ensemble des études sur le long terme, « la pureté de l’aspartame utilisé dans ces études est considéré comme étant de 100% »34.
La crédibilité de cette réévaluation de 2013 est aussi fragilisée par la révélation des liens de plusieurs experts de l’EFSA avec l’industrie de l’aspartame57,59,62. Ces conflits d’intérêts ont conduit à l’adoption en 2019 d’une loi européenne visant à renforcer la transparence et l’intégrité scientifique au sein de l’EFSA65,116. Une avancée, certes, mais qui n’a jamais conduit à rouvrir le dossier ni à réexaminer la DJA de l’aspartame.
En 2023, le JECFA a, lui aussi, choisi de maintenir la DJA de l’aspartame inchangée114,117. Là encore, sa conclusion repose largement sur l’étude de 1981 financée par le fabricant Ajinomoto118.
Cependant, plusieurs acteurs — parmi lesquels l’ONG européenne Foodwatch119 et l’ONG américaine U.S. Right to Know120 — ont relevé au sein du JECFA les mêmes dérives que celles reprochées à l’EFSA : une sélection biaisée des études, la présence de six experts membres du comité travaillant parallèlement à l’ILSI, ainsi que de sérieuses lacunes dans la politique de transparence et de gestion des conflits d’intérêts.
Des risques majeurs exclus des critères d’évaluation
En plus de s’appuyer sur des études anciennes et controversées, la DJA de l’aspartame fixée en Europe repose sur des travaux qui ne couvrent pas l’ensemble des effets toxiques potentiels de cette substance.
Pour établir une DJA, les autorités sanitaires se basent uniquement sur des études menées sur des animaux (rats, souris ou lapins) exposés pendant deux ans à une substance dont la composition et la pureté sont censées être parfaitement connues. Les effets pris en compte sont uniquement ceux visibles lors d’examens biologiques, tels que : variations de poids, anomalies dans la formation ou le fonctionnement des organes, impacts sur la reproduction ou la fertilité, effets sur la descendance, apparition de tumeurs ou autres anomalies.
Cependant, ces modèles animaux ne permettent pas toujours d’identifier tous les effets néfastes chez l’humain. Certains impacts — sur le comportement, la mémoire, l’appétit, ou encore les effets dits « cocktail » liés à l’exposition simultanée à d’autres substances courantes (médicaments, additifs, pesticides, etc.) — sont difficiles, voire impossibles, à détecter avec cette approche. Cette limite conduit ainsi probablement à sous-estimer certains risques, notamment la possible neurotoxicité de l’aspartame, ou le développement progressif d’une résistance à l’insuline. L’OMS rappelle d’ailleurs, en introduction de son rapport de 202275, que « les effets à long terme sur la santé de la consommation d’édulcorants à des niveaux inférieurs à la DJA ne sont pas bien caractérisés ».
Par ailleurs, les données issues d’études sur l’humain ne sont pas prises en compte lors de l’établissement des DJA121. En effet, ces seuils sont généralement fixés au moment où une nouvelle substance obtient son autorisation de mise sur le marché. Or, si des essais cliniques sur l’homme sont obligatoires pour les médicaments, ce n’est pas le cas pour les additifs alimentaires. D’un point de vue éthique, il serait difficile de justifier qu’un groupe de volontaires soit exposé à une molécule inédite uniquement pour valider sa commercialisation, surtout qu’un additif alimentaire n’apporte pas le même bénéfice qu’un médicament. Les données humaines sont donc examinées après coup, principalement via des études épidémiologiques. Celles-ci cherchent à déterminer, une fois l’additif déjà autorisé, si les consommateurs réguliers présentent une fréquence plus élevée de certaines maladies que la population générale. Plusieurs scientifiques sont allés jusqu’à qualifier la DJA de « procédure artisanale fondée à la fois sur la science et sur des postulats »122 et ont appelé à une meilleure prise en compte des données humaines123.
Plusieurs études épidémiologiques – menées chez l’humain – ont ainsi mis en évidence des effets nocifs de l’aspartame à des doses pourtant autorisées, couramment consommées et très inférieures à la DJA. Ces recherches mettent par exemple en évidence une augmentation du risque de cancers124, de maladies cardiovasculaires125 et de diabète de type 2126, à des doses près de 200 fois inférieures à la DJA, soit l’équivalent d’une demi-canette de soda par jour. Un risque accru d’obésité127, ainsi qu’un poids de naissance plus élevé chez les nouveau-nés128, ont également été constatés pour les personnes consommant un seul soda « sans sucre » par jour. Ces études ne sont cependant pas prises en compte dans le calcul de la DJA, car elles ne permettent pas de déterminer une dose sans risque, contrairement aux études menées sur l’animal.
De plus, lors de la réévaluation par l’EFSA en 201334, les études animales portant sur des risques émergents — comme les effets sur le microbiote intestinal — n’étaient pas prises en compte. Or, ces risques sont aujourd’hui considérés comme préoccupants, compte tenu des conséquences potentiellement graves qu’une perturbation du microbiote liée à l’aspartame pourrait engendrer129.
Le seuil actuel de la DJA est donc incomplet et ne protège pas pleinement la santé des populations, ce qui rend l’absence de révision de la DJA d’autant plus préoccupante.
Un édulcorant sans bénéfice sur le poids
Depuis son autorisation, l’aspartame est présenté comme une alternative au sucre permettant de réduire les apports caloriques et de mieux contrôler son poids. Cet argument peut sembler logique sur le papier.
Cependant, de plus en plus d’études remettent en cause cette promesse. L’ANSES (Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail) a publié en 2015 un rapport s’appuyant sur 383 publications scientifiques130. Elle y conclut que les édulcorants, y compris l’aspartame, n’ont démontré aucun effet bénéfique sur la perte de poids ni sur le contrôle de la glycémie. Ces résultats concernent aussi bien les personnes en bonne santé que celles atteintes de diabète.
Les conclusions de l’ANSES rejoignent celles du rapport de l’OMS publié en 202275. En effet, les études à court terme (moins de 12 mois) suggèrent un faible effet de réduction du poids ou du tour de taille chez les personnes cherchant à perdre du poids131. Cependant, à plus long terme, les études de cohorte menées sur 4 à 9 ans révèlent une tendance inverse : une consommation plus élevée d’édulcorants est associée à une augmentation de 2,6 cm du tour de taille132. L’OMS rapporte même qu’une consommation régulière d’édulcorants est associée à une augmentation de 76 % du risque d’obésité, ainsi qu’à une hausse significative de l’indice de masse corporelle (IMC). En conclusion, l’OMS préconise clairement de « ne pas utiliser d’édulcorants à des fins de perte de poids ». Chez l’enfant, l’ANSES note également que la majorité des études de suivi à long terme mettent en évidence, de façon paradoxale, un lien entre une consommation régulière d’édulcorants et la prise de poids133.
Plus préoccupant encore : une étude canadienne de 2020128, menée sur plus de 2 200 femmes enceintes, montre que les bébés exposés à l’aspartame in utero présentent un poids significativement plus élevé à la naissance que ceux non exposés. Ces bébés présentent également un risque accru de complications métaboliques, comme une résistance à l’insuline ou une accumulation de graisse dans les tissus, des facteurs qui augmentent leur vulnérabilité à la prise de poids ultérieure et favorisent le développement de l’obésité dès l’enfance ou à l’âge adulte.
Le mécanisme exact derrière cet effet reste encore mal compris. Plusieurs pistes sont envisagées : une activation inappropriée des récepteurs du goût sucré, une altération de la tolérance au glucose134, le développement progressif d’une résistance à l’insuline ou la perturbation du microbiote intestinal135.
Conclusion
Le principe de précaution est au cœur du système de réglementation européen, où il est inscrit dans la loi depuis 2002136. Pourtant, l’histoire de l’aspartame montre à quel point ce principe peut être affaibli lorsque l’évaluation des risques est noyée sous l’influence des lobbies industriels.
La question n’est donc plus seulement de savoir si l’aspartame présente un risque pour la santé, mais bien de savoir si nos autorités sont encore en mesure de protéger efficacement les consommateurs.
Face à cette situation, il est essentiel de faire entendre une voix claire : les intérêts économiques ne doivent pas dicter les décisions qui concernent la santé publique. C’est le sens de la pétition portée par Yuka, Foodwatch et La Ligue contre le cancer, qui demande à la Commission européenne d’interdire l’aspartame. La santé ne devrait jamais être la variable d’ajustement des intérêts économiques.
- ¹ Valavanidis, 2023. Aspartame, Artificial Sweetener, Credible Evidence that is Potentially Carcinogenic? IARC will decide in 2023 if an increased risk of cancer is associated with Aspartame consumption. https://www.researchgate.net/profile/Athanasios-Valavanidis/publication/372344870_Aspartame_Artificial_Sweetener_Credible_Evidence_that_is_Potentially_Carcinogenic_IARC_will_decide_in_2023_if_an_increased_risk_of_cancer_is_associated_with_Aspartame_consumption/links/64b11080c41fb852dd6ff270/Aspartame-Artificial-Sweetener-Credible-Evidence-that-is-Potentially-Carcinogenic-IARC-will-decide-in-2023-if-an-increased-risk-of-cancer-is-associated-with-Aspartame-consumption.pdf
- ² Shaher et al, 2023. Aspartame Safety as a Food Sweetener and Related Health Hazards. https://www.mdpi.com/2072-6643/15/16/3627
- ³ Market prices: aspartame USD 10,49 per kg (https://www.imarcgroup.com/aspartame-pricing-report
- (Germany)), sugar USD 0,5 per kg (https://www.statista.com/statistics/675828/average-prices-sugar-worldwide/
- ). Achieving same sweetness (aspartame 200x that of sugar) USD 0,5 for sugar and USD 0,05 for aspartame needed (calculation made on December 6, 2024).
- ⁴ Czarnecka et al, 2021. Aspartame—True or False? Narrative Review of Safety Analysis of General Use in Products. Nutrients. 2021 Jun 7;13(6):1957. https://pmc.ncbi.nlm.nih.gov/articles/PMC8227014/
- ⁵ Food and Drug Administration, 1974. Rules and Regulations. Federal Register, vol. 39, no. 145 - Friday, July 26, 1974. https://archives.federalregister.gov/issue_slice/1974/7/26/27316-27320.pdf#page=2
- ⁶ Mission Possible, 2006. Report for schools, ob-gyn and pediatricians on children and aspartame/MSG. Prepared By Mission Possible, Dr. Betty Martini. https://citeseerx.ist.psu.edu/document?repid=rep1&type=pdf&doi=d0041fbf9e37d3c641bab2a336221cf41a9933bd
- ⁷ Food and Drug Administration, 1975. Rules and Regulations. Federal Register, vol. 40, no. 235 - Friday, December 5, 1975. https://archives.federalregister.gov/issue_slice/1975/12/5/56899-56910.pdf
- ⁸ Committee on Toxicity of Chemicals in Food, Consumer Products and the Environment, 1990. Aspartame - Validity of Searle toxicity studies. TOX/90/44. https://data.parliament.uk/DepositedPapers/Files/DEP2013-0273/8TOX9044.pdf
- ⁹ Swankin and Turner. Aspartame / NutraSweet, The History of the Aspartame Controversy. http://www.swankin-turner.com/hist.html
- ¹⁰ The Guardian, 2005. Safety of artificial sweetener called into question by MP. https://www.theguardian.com/politics/2005/dec/15/foodanddrink.immigrationpolicy
- ¹¹ Blaylock, 2006. Aspartame Is An Excitoneurotoxic Carcinogenic Drug! https://citeseerx.ist.psu.edu/document?repid=rep1&type=pdf&doi=eef405cbc0079082949016cd279a13a542588958
- ¹² Mullarkey and Newman, 1994. Sweet Delusion. How safe is your artificial sweetener ? Part one: the hidden history of Aspartame. https://ia800109.us.archive.org/11/items/OnAspartameMsg/SweetDelusion.pdf
- ¹³ Broer, 2002. Aspartame: a chronicle of crime. Fit at forty-sixty and beyond. The in-depth health and nutrition analysis. Vol. 1, no 2, article 3. https://irp.cdn-website.com/6b820530/files/uploaded/Aspartame%20Dangers.pdf
- ¹⁴ Smyth, 1983. The FDA’s Public Board of Inquiry and the Aspartame Decision. Indiana Law Journal, vol. 58, issue 4. https://www.repository.law.indiana.edu/cgi/viewcontent.cgi?article=2268&context=ilj
- ¹⁵ Nill, 2000. The History of Aspartame. Harvard Library. https://dash.harvard.edu/server/api/core/bitstreams/7312037c-a98d-6bd4-e053-0100007fdf3b/content
- ¹⁶ UK Parliament. Artificial Sweeteners. 14 Dec 2005 : Column 491WH-continued. https://publications.parliament.uk/pa/cm200506/cmhansrd/vo051214/halltext/51214h05.htm
- ¹⁷ Food and Drug Administration, 1981. Federal Register, vol. 46, no. 142, Friday, July 24, 1981, Notices. https://archives.federalregister.gov/issue_slice/1981/7/24/38256-38289.pdf#page=30
- ¹⁸ Sykes, 2015. The Aspartame Controversy of 1981. The Hidden Truth Behind the Not-So-Sweet Artificial Sweetener. https://vtechworks.lib.vt.edu/server/api/core/bitstreams/a814bc16-5c18-4e53-82eb-6472e092e7af/content
- ¹⁹ Shapiro, 1986. Scientific Issues and the Function of Hearing Procedures: Evaluating the FDA’s Public Board of Inquiry. https://scholarship.law.duke.edu/cgi/viewcontent.cgi?article=2944&context=dlj
- ²⁰ Millstone, 2019. Aspartame Chronology. https://www.sussex.ac.uk/webteam/gateway/file.php?name=doc-3---chronology-metzenbaum-1986002.pdf&site=25
- ²¹ Ishii, 1981. Incidence of brain tumors in rats fed aspartame. Toxicology Letters. 1981 Mar;7(6):433-7.https://pubmed.ncbi.nlm.nih.gov/7245229/
- ²² Ishii et al, 1981. Toxicity of aspartame and its diketopiperazine for Wistar rats by dietary administration for 104 weeks. Toxicology, 1981;21(2):91-4. https://pubmed.ncbi.nlm.nih.gov/7281205/
- ²³ Soffritti et al, 2014. The Carcinogenic Effects of Aspartame: The Urgent Need for Regulatory Re-Evaluation. American Journal of industrial Medicine. 57:383–397 (2014). https://www.ramazzini.org/wp-content/uploads/2009/02/The-carcinogenic-effects-of-aspartame_The-urgent-need-for-regulatory-re-evaluation-2014.pdf
- ²⁴ National Cancer Institute, 1976. Guideline for Carcinogen Bioassay in Small Rodents. NCI-CG-TR-1. https://ntp.niehs.nih.gov/sites/default/files/ntp/htdocs/lt_rpts/tr001.pdf
- ²⁵ Jacobs and Hatfield, 2012. History of Chronic Toxicity and Animal Carcinogenicity Studies for Pharmaceuticals. Veterinary Pathology. 2012;50(2):324-333. https://journals.sagepub.com/doi/10.1177/0300985812450727
- ²⁶ Condon, 1981. Memorandum: Aspartame- Dissenting Opinion on the Brain Tumor Issue. May. 19, 1981. https://www.sussex.ac.uk/webteam/gateway/file.php?name=doc-18---condon-to-levitt-19may1981.pdf&site=25
- ²⁷ Government Accountability Office, 1986. Six Former HHS Employees’s Involvement in Aspartame’s Approval. Food and Drug Administration. Briefing report to the Honorable Howard Metzenbaum United State Senate. https://www.gao.gov/assets/hrd-86-109br.pdf
- ²⁸ The Ecologist, 2005. Aspartame. September 2005. https://h2rc2.com/Ecogypt/page1/page17/assets/AspartameResearch.pdf
- ²⁹ Huffpost, 2011. Donald Rumsfeld and the Strange History of Aspartame. https://www.huffpost.com/entry/donald-rumsfeld-and-the-s_b_805581
- ³⁰ Food and Drug Administration, 2020. Arthur Hull Hayes. https://www.fda.gov/about-fda/fda-leadership-1907-today/arthur-hayes
- ³¹ Government of Canada, 2023. L’aspartame. https://www.canada.ca/fr/sante-canada/services/aliments-nutrition/salubrite-aliments/additifs-alimentaires/succedanes-sucre/aspartame-edulcorants-artificiels.html
- ³² news.com.au. ‘Increased risk’: Warning over cult diet drinks after animal study. https://www.news.com.au/lifestyle/health/health-problems/warning-over-cult-diet-drink-revealed/news-story/58b3bea834a099dc9bf2fbef3d65d266
- ³³ European Food Safety Authority, 2011. EFSA publishes original industry studies on aspartame. https://www.efsa.europa.eu/en/press/news/111124-0
- ³⁴ European Food Safety Authority, 2013. Scientific Opinion on the re-evaluation of aspartame (E 951) as a food additive. EFSA Journal 2013;11(12):3496. https://efsa.onlinelibrary.wiley.com/doi/epdf/10.2903/j.efsa.2013.3496
- ³⁵ European Food Safety Authority, 2023. Aspartame. https://www.efsa.europa.eu/en/topics/topic/aspartame
- ³⁶ Millstone et Dawson, 2019. EFSA’s toxicological assessment of aspartame: was it even-handedly trying to identify possible unreliable positives and unreliable negatives? Arch Public Health 77, 34 (2019). https://archpublichealth.biomedcentral.com/articles/10.1186/s13690-019-0355-z
- ³⁷ Martini, 1997. Researchers call for further studies after identifying a possible link between aspartame and brain tumors. https://www.sott.net/article/149206-Dr-John-Olney-on-Brain-tumors-and-aspartame
- ³⁸ Mandrioli et al, 2016. Relationship between Research Outcomes and Risk of Bias, Study Sponsorship, and Author Financial Conflicts of Interest in Reviews of the Effects of Artificially Sweetened Beverages on Weight Outcomes: A Systematic Review of Reviews. PLoS One. 2016 Sep 8;11(9):e0162198. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5015869/
- ³⁹ Azad et al, 2017. Nonnutritive sweeteners and cardiometabolic health: a systematic review and meta-analysis of randomized controlled trials and prospective cohort studies. CMAJ. 2017 Jul 17;189(28):E929-E939. https://pmc.ncbi.nlm.nih.gov/articles/PMC5515645/
- ⁴⁰ Soffritti et al, 2005. First Experimental Demonstration of the Multipotential Carcinogenic Effects of Aspartame Administered in the Feed to Sprague-Dawley Rats. Environmental Health Perspectives Volume 114, Issue 3. Pages 379 - 385. https://ehp.niehs.nih.gov/doi/abs/10.1289/ehp.8711
- ⁴¹ Belpoggi et al, 2006. Results of Long-Term Carcinogenicity Bioassay on Sprague-Dawley Rats Exposed to Aspartame Administered in Feed. Annals of the New york Academy of Sciences. https://nyaspubs.onlinelibrary.wiley.com/doi/abs/10.1196/annals.1371.080
- ⁴² Soffritti et al, 2007. Life-Span Exposure to Low Doses of Aspartame Beginning during Prenatal Life Increases Cancer Effects in Rats. Environmental Health Perspectives, Volume 115, Issue 9, Pages 1293 - 129. https://ehp.niehs.nih.gov/doi/full/10.1289/ehp.10271
- ⁴³ Huff, 2006. Chemicals Studied and Evaluated in Long-Term Carcinogenesis Bioassays by Both the Ramazzini Foundation and the National Toxicology Program. Annuals of the New York Academy of Sciences, Volume 982, Issue 1. https://nyaspubs.onlinelibrary.wiley.com/doi/10.1111/j.1749-6632.2002.tb04935.x
- ⁴⁴ The Organisation for Economic Co-operation and Development, 2018. OECD 451. OECD Guideline for the testing of Chemicals: Carcinogenicity Studies. https://www.oecd.org/content/dam/oecd/en/publications/reports/2018/06/test-no-451-carcinogenicity-studies_g1gh2955/9789264071186-en.pdf
- ⁴⁵ European Food Safety Authority, 2006. EFSA assesses new aspartame study and reconfirms its safety. https://www.efsa.europa.eu/en/news/efsa-assesses-new-aspartame-study-and-reconfirms-its-safety
- ⁴⁶ Soffritti et al, 2014. The Carcinogenic Effects of Aspartame: The Urgent Need for Regulatory Re-Evaluation. American Jounal of Industral Medicine 57:383–397 (2014). https://www.ramazzini.org/wp-content/uploads/2009/02/The-carcinogenic-effects-of-aspartame_The-urgent-need-for-regulatory-re-evaluation-2014.pdf
- ⁴⁷ Huff et al, 2016. The limits of two-year bioassay exposure regimens for identifying chemical carcinogens. Environ Health Perspect. 2008 Nov;116(11):1439-42. https://pubmed.ncbi.nlm.nih.gov/19057693/
- ⁴⁸ Landrigan and Straif, 2021. Aspartame and cancer – new evidence for causation. Environ Health 20, 42 (2021). https://ehjournal.biomedcentral.com/articles/10.1186/s12940-021-00725-y
- ⁴⁹ Gnudi et al, 2023. Hemolymphoreticular Neoplasias from the Ramazzini Institute Long-term Mice and Rat Studies on Aspartame. Annals of Global Health, 89(1), p. 43. https://annalsofglobalhealth.org/articles/10.5334/aogh.4163
- ⁵⁰ International Agency for Research on Cancer, 2024. Aspartame, Methyleugenol, and Isoeugenol IARC Monographs on the Identification of Carcinogenic Hazards to Humans Volume 134. https://publications.iarc.who.int/627
- ⁵¹ Magnuson et al, 2007. Aspartame: a safety evaluation based on current use levels, regulations, and toxicological and epidemiological studies. Crit Rev Toxicol. 2007;37(8):629-727. https://pubmed.ncbi.nlm.nih.gov/17828671/
- ⁵² Aspartame.org, 2006. Comprehensive Review of Ramazzini Study Demonstrates No Scientific Evidence of Aspartame and Cancer Link. https://aspartame.org/comprehensive-review-ramazzini-study-demonstrates-no-scientific-evidence-aspartame-cancer-link/
- ⁵³ Soffritti, 2008. Carcinogenicity of Aspartame: Soffritti Responds. Environmental Health Perspectives, Volume 116, Issue 6, Page A240. https://ehp.niehs.nih.gov/doi/full/10.1289/ehp.10881R
- ⁵⁴ Collegium Ramazzini, 2011. Confirmation of the Experimental Carcinogenicity of Aspartame. https://collegiumramazzini.org/news/detail/211
- ⁵⁵ Center for Science in the Public Interest, 2013. Evaluation of Ramazzini Institute Aspartame Studies – and EFSA’s Assessment. Lisa Y. Lefferts, MSPH Senior Scientist. https://www.efsa.europa.eu/sites/default/files/event/documentset/130409-p06.pdf
- ⁵⁶ Foodwatch, 2025. Clean Washing Aspartame. Why aspartame needs to be banned, based on independent science. https://www.foodwatch.org/fileadmin/-INT/additives/2025-02-04_foodwatch-report-aspartame.pdf
- ⁵⁷ Réseau Environnement Santé, 2013. Analyse du rapport EFSA “Draft Opinion on the Re-Evaluation of Aspartame (E 951) as a Food Additive” https://reseau-environnement-sante.fr/wp-content/uploads/2016/01/AnalyseRapport-EFSAJanv2013-VF.pdf
- ⁵⁸ Marie-Monique Robin, 2011. Extract of the movie « Our Daily Poison » - https://www.youtube.com/watch?v=3CBXDU4cKNE
- ⁵⁹ Corporate Europe Observatory, 2011. Exposed: conflicts of interest among EFSA’s experts on food additives. https://corporateeurope.org/sites/default/files/publications/efsa_ans_panel.pdf
- ⁶⁰ U.S. Right to Know, 2023. International Life Sciences Institute (ILSI) is a food industry lobby group. September 16, 2023. https://usrtk.org/pesticides/ilsi-is-a-food-industry-lobby-group/
- ⁶¹ European Parliament, 2014. REPORT on discharge in respect of the implementation of the budget of the European Food Safety Authority for the financial year 2012. A7-0219/2014. https://www.europarl.europa.eu/doceo/document/A-7-2014-0219_EN.html?redirect
- ⁶² Corporate Europe Observatory, 2020. Conflicts of interest scandals at EFSA: A non-exhaustive chronology of recent events. https://corporateeurope.org/en/food-and-agriculture/efsa/chronology
- ⁶³ European Food Safety Authority, 2014. Decision of the Executive Director on Declarations of Interest. EFSA/LRA/DEC/02/2014. https://www.efsa.europa.eu/sites/default/files/corporate_publications/files/independencerules2014.pdf
- ⁶⁴ European Food Safety Authority, 2015. Increasing robustness, transparency and openness of scientific assessments. https://efsa.onlinelibrary.wiley.com/doi/epdf/10.2903/j.efsa.2015.e13031
- ⁶⁵ Regulation (EU) 2019/1381 of the European Parliament and of the Council - https://eur-lex.europa.eu/legal-content/EN/TXT/?uri=uriserv:OJ.L_.2019.231.01.0001.01.ENG&toc=OJ:L:2019:231:TOC
- ⁶⁶ Soffritti et al, 2014. The Carcinogenic Effects of Aspartame: The Urgent Need for Regulatory Re-Evaluation. American Journal of Industrial Medicine. https://www.ramazzini.org/wp-content/uploads/2009/02/The-carcinogenic-effects-of-aspartame_The-urgent-need-for-regulatory-re-evaluation-2014.pdf
- ⁶⁷ Doueihy et al, 2025. Aspartame and Human Health: A Mini-Review of Carcinogenic and Systemic Effects. J Xenobiot. 2025 Jul 7;15(4):114. https://pmc.ncbi.nlm.nih.gov/articles/PMC12286081/#notes2
- ⁶⁸ Le Point, 2011. Aspartame, un scandale sanitaire en cours. https://www.lepoint.fr/sante/aspartame-un-scandale-sanitaire-en-cours-15-09-2011-1373463_40.php
- ⁶⁹ International Agency for Research on Cancer, 2024. IARC Monographs Volume 134: Aspartame, methyleugenol, and isoeugenol. 13 September 2024. https://www.iarc.who.int/news-events/iarc-monographs-volume-134-aspartame-methyleugenol-and-isoeugenol/
- ⁷⁰ International Agency for Research on Cancer, 2024. Aspartame, methyleugenol, and isoeugenol. IARC Monographs on the Identification of Carcinogenic Hazards to Humans, No. 134. https://www.ncbi.nlm.nih.gov/books/NBK609291/
- ⁷¹ Debras et al, 2022. Artificial sweeteners and cancer risk: Results from the NutriNet-Santé population-based cohort study. PLoS Med. 2022 Mar 24;19(3):e1003950. https://journals.plos.org/plosmedicine/article?id=10.1371/journal.pmed.1003950
- ⁷² Schernhammer et al, 2012. Consumption of artificial sweetener- and sugar-containing soda and risk of lymphoma and leukemia in men and women. Am J Clin Nutr. 2012 Dec;96(6):1419-28. https://www.sciencedirect.com/science/article/pii/S0002916523029209?via%3Dihub
- ⁷³ Landrigan et al, 2025. Irregularities in the IARC Working Group Evaluation of Ramazzini Institute Aspartame Studies. Ann Glob Health. 2025 Jun 6;91(1):28. https://pmc.ncbi.nlm.nih.gov/articles/PMC12143253/
- ⁷⁴ World Health Organization, 2024. Diabetes. https://www.who.int/news-room/fact-sheets/detail/diabetes
- ⁷⁵ World Health Organization, 2022. Health effects of the use of non-sugar sweeteners: a systematic review and meta-analysis. https://www.who.int/publications/i/item/9789240046429
- ⁷⁶ Fagherazzi et al, 2013. Consumption of artificially and sugar-sweetened beverages and incident type 2 diabetes in the Etude Epidemiologique aupres des femmes de la Mutuelle Generale de l'Education Nationale-European Prospective Investigation into Cancer and Nutrition cohort. Am J Clin Nutr. 2013 Mar;97(3):517-23. https://www.sciencedirect.com/science/article/pii/S0002916523054412?via%3Dihub
- ⁷⁷ Nettleton et al, 2009. Diet soda intake and risk of incident metabolic syndrome and type 2 diabetes in the Multi-Ethnic Study of Atherosclerosis (MESA). Diabetes Care. 2009 Apr;32(4):688-94. https://pmc.ncbi.nlm.nih.gov/articles/PMC2660468/
- ⁷⁸ Sakurai et al, 2014. Sugar-sweetened beverage and diet soda consumption and the 7-year risk for type 2 diabetes mellitus in middle-aged Japanese men. Eur J Nutr. 2014 Feb;53(1):251-8. doi: 10.1007/s00394-013-0523-9. https://pubmed.ncbi.nlm.nih.gov/23575771/
- ⁷⁹ Gul et al, 2017. Inhibition of the gut enzyme intestinal alkaline phosphatase may explain how aspartame promotes glucose intolerance and obesity in mice. Appl Physiol Nutr Metab. 2017 Jan;42(1):77-83. https://cdnsciencepub.com/doi/full/10.1139/apnm-2016-0346
- ⁸⁰ Fowler et al, 2012. Fueling the obesity epidemic? Artificially sweetened beverage use and long-term weight gain. Obesity (Silver Spring). 2008 Aug;16(8):1894-900. https://onlinelibrary.wiley.com/doi/full/10.1038/oby.2008.284
- ⁸¹ Anton et al, 2010. Effects of stevia, aspartame, and sucrose on food intake, satiety, and postprandial glucose and insulin levels. Appetite. 2010 Aug;55(1):37-43. https://www.sciencedirect.com/science/article/abs/pii/S0195666310000826
- ⁸² Suez et al, 2022. Personalized microbiome-driven effects of non-nutritive sweeteners on human glucose tolerance. Cell. 2022 Sep 1;185(18):3307-3328.e19. https://www.cell.com/cell/fulltext/S0092-8674(22)00919-9
- ⁸³ Debras et al, 2023. Artificial Sweeteners and Risk of Type 2 Diabetes in the Prospective NutriNet-Santé Cohort. Diabetes Care. 2023 Sep 1;46(9):1681-1690. https://pmc.ncbi.nlm.nih.gov/articles/PMC10465821/
- ⁸⁴ Malik and Hu, 2012. Sweeteners and Risk of Obesity and Type 2 Diabetes: The Role of Sugar-Sweetened Beverages. Curr Diab Rep. 2012 Jan 31. https://link.springer.com/article/10.1007/s11892-012-0259-6
- ⁸⁵ World Health Organization, 2025. Cardiovascular diseases (CVDs). https://www.who.int/news-room/fact-sheets/detail/cardiovascular-diseases-(cvds)
- ⁸⁶ Debras et al, 2022. Artificial sweeteners and risk of cardiovascular diseases: results from the prospective NutriNet-Santé cohort. BMJ. 2022 Sep 7;378:e071204. https://www.bmj.com/content/378/bmj-2022-071204.full
- ⁸⁷ World Health Organization, 2023. Use of non-sugar sweeteners. WHO guideline. https://iris.who.int/bitstream/handle/10665/367660/9789240073616-eng.pdf?sequence=1
- ⁸⁸ Zhang et al, 2025. Aspartame and ischemic stroke: unraveling the molecular link through network toxicology and molecular docking analysis. Sci Rep. 2025 Jul 4;15(1):23871. https://www.nature.com/articles/s41598-025-08898-z
- ⁸⁹ Valdes et al, 2018. Role of the gut microbiota in nutrition and health. BMJ. 2018 Jun 13;361:k2179. https://www.bmj.com/content/361/bmj.k2179
- ⁹⁰ Qin et al, 2012. A Metagenome-Wide Association Study of the Gut Microbiome and Metabolic Syndrome. Front Microbiol. 2021 Jul 16;12:682721. https://www.nature.com/articles/nature11450
- ⁹¹ Huybrechts et al, 2021. The Human Microbiome in Relation to Cancer Risk: A Systematic Review of Epidemiologic Studies. Cancer Epidemiol Biomarkers Prev. 2020 Oct;29(10):1856-1868. https://pmc.ncbi.nlm.nih.gov/articles/PMC7541789/#S15
- ⁹² Tang et al, 2013. Intestinal microbial metabolism of phosphatidylcholine and cardiovascular risk. N Engl J Med. 2013 Apr 25;368(17):1575-84. https://www.nejm.org/doi/full/10.1056/NEJMoa1109400
- ⁹³ Baothman et al, 2016. The role of Gut Microbiota in the development of obesity and Diabetes. Lipids Health Dis. 2016 Jun 18;15:108. https://link.springer.com/article/10.1186/s12944-016-0278-4
- ⁹⁴ Suez et al, 2014. Artificial sweeteners induce glucose intolerance by altering the gut microbiota. Nature. 2014 Oct 9;514(7521):181-6. https://pubmed.ncbi.nlm.nih.gov/25231862/
- ⁹⁵ Palmnäs et al, 2014. Low-dose aspartame consumption differentially affects gut microbiota-host metabolic interactions in the diet-induced obese rat. PLoS One. 2014 Oct 14;9(10):e109841. https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0109841
- ⁹⁶ Shil et al, 2020. Artificial Sweeteners Disrupt Tight Junctions and Barrier Function in the Intestinal Epithelium through Activation of the Sweet Taste Receptor, T1R3. Nutrients. 2020 Jun 22;12(6):1862. https://pmc.ncbi.nlm.nih.gov/articles/PMC7353258/
- ⁹⁷ Pepino, 2016. Metabolic effects of non-nutritive sweeteners. Physiol Behav. 2015 Dec 1;152(Pt B):450-5. https://pmc.ncbi.nlm.nih.gov/articles/PMC4661066/
- ⁹⁸ Rother et al, 2018. How Non-nutritive Sweeteners Influence Hormones and Health. Trends Endocrinol Metab. 2018 Jul;29(7):455-467. https://pubmed.ncbi.nlm.nih.gov/29859661/
- ⁹⁹ Angelin et al, 2024. Artificial sweeteners and their implications in diabetes: a review. Front Nutr. 2024 Jun 25;11:1411560. https://pmc.ncbi.nlm.nih.gov/articles/PMC11233937/#B5
- ¹⁰⁰ Olney and Ho, 1970. Brain damage in infant mice following oral intake of glutamate, aspartate or cysteine. Nature. 1970 Aug 8;227(5258):609-11. https://www.nature.com/articles/227609b0
- ¹⁰¹ Olney, 1979. Excitotoxic Amino Acids: Research Applications and Safety Implications. https://www.ajinomoto.com.my/sites/default/files/paragraph/side-by-side/files/excitotoxic-amino-acids.pdf
- ¹⁰² Humphries et al, 2008. Direct and indirect cellular effects of aspartame on the brain. Eur J Clin Nutr. 2008 Apr;62(4):451-62. https://www.nature.com/articles/1602866
- ¹⁰³ Choudhar and Lee, 2018. The debate over neurotransmitter interaction in aspartame usage. J Clin Neurosci. 2018 Oct;56:7-15. https://www.sciencedirect.com/science/article/abs/pii/S0967586818305770
- ¹⁰⁴ Ashok et al, 2015. Neurobehavioral changes and activation of neurodegenerative apoptosis on long-term consumption of aspartame in the rat brain. Journal of Nutrition & Intermediary Metabolism, Vol. 2, Issues 3-4, December 2015, Pages 76-85. https://www.sciencedirect.com/science/article/pii/S2352385915300025
- ¹⁰⁵ Jones et al, 2023. Learning and memory deficits produced by aspartame are heritable via the paternal lineage. Sci Rep. 2023 Aug 31;13(1):14326. https://www.nature.com/articles/s41598-023-41213-2
- ¹⁰⁶ Bai et al, 2024. Non-nutritive Sweetener Aspartame Disrupts Circadian Behavior and Causes Memory Impairment in Mice. J Agric Food Chem. 2024 Oct 23;72(42):23478-23492. https://pubmed.ncbi.nlm.nih.gov/39382230/
- ¹⁰⁷ European Food Safety Authority, 2025. ADI. https://www.efsa.europa.eu/en/glossary/adi
- ¹⁰⁸ Joint FAO/WHO Expert Committee on Food Additives, 1980. Evaluation of certain food additive. Twenty-fourth Report of the Joint FAO/WHO Expert Committee on Food Additives. https://iris.who.int/bitstream/handle/10665/41410/WHO_TRS_653.pdf?sequence=1
- ¹⁰⁹ Food and Drug Administration, 2023. Timeline of Selected FDA Activities and Significant Events Addressing Aspartame. https://www.fda.gov/food/food-additives-petitions/timeline-selected-fda-activities-and-significant-events-addressing-aspartame
- ¹¹⁰ Gordon 1987. News Story. https://www.sussex.ac.uk/webteam/gateway/file.php?name=document-24-greg-gordon-upi-12oct1987.pdf&site=25
- ¹¹¹ Food and Drug Administration, 2023. Timeline of Selected FDA Activities and Significant Events Addressing Aspartame. https://www.fda.gov/food/food-additives-petitions/timeline-selected-fda-activities-and-significant-events-addressing-aspartame
- ¹¹² Scientific Committee for Food, 1984. Reports of the Scientific Committee for Food (Sixteenth Series). https://ec.europa.eu/food/fs/sc/scf/reports/scf_reports_16.pdf
- ¹¹³ European Food Safety Authority, 2013. Scientific Opinion on Aspartame. https://www.efsa.europa.eu/sites/default/files/corporate_publications/files/factsheetaspartame.pdf
- ¹¹⁴ World Health Organization, 2023. Evaluations of the Joint FAO/WHO Expert Committee on FDood Additives (JECFA). Aspartame. https://apps.who.int/food-additives-contaminants-jecfa-database/Home/Chemical/62
- ¹¹⁵ World Health Organization, 2023. Aspartame hazard and risk assessment results released. https://www.who.int/news/item/14-07-2023-aspartame-hazard-and-risk-assessment-results-released
- ¹¹⁶ French Agency for Food, Environmental and Occupational Health & Safety, 2021. The European Transparency Regulation: a new framework for risk assessment and food safety. https://www.anses.fr/en/content/european-transparency-regulation-new-framework-risk-assessment-and-food-safety
- ¹¹⁷ Joint FAO/WHO Expert Committee on Food Additives, 2023. Evaluation of certain food additives? Ninety-sixth report of the Joint FAO/WHO Expert Committee on Food Additives. https://iris.who.int/bitstream/handle/10665/376279/9789240083059-eng.pdf?sequence=1
- ¹¹⁸ Joint FAO/WHO Expert Committee on Food Additives, 2024. Comité du codex sur les additifs alimentaires. Questions d’intérêt découlant de la FAO et l’OMS et des 96ème et 97ème réunions du Comité mixte FAO/OMS d’Experts des Additifs Alimentaires (JECFA) respectivement. https://www.fao.org/fao-who-codexalimentarius/sh-proxy/en/?lnk=1&url=https%253A%252F%252Fworkspace.fao.org%252Fsites%252Fcodex%252FMeetings%252FCX-711-54%252FWorking%2Bdocuments%252Ffa54_03f.pdf
- ¹¹⁹ Foodwatch, 2025. Clean Washing Aspartame. Why aspartame needs to be banned, based on
- independent science. https://www.foodwatch.org/fileadmin/-INT/additives/2025-02-04_foodwatch-report-aspartame.pdf
- ¹²⁰ U.S. Right to Know, 2023. Did a Coca-Cola front group sway a WHO review of Aspartame ? Gary Ruskin, July 19, 2023. https://usrtk.org/sweeteners/coca-cola-front-group-who-review-of-aspartame/
- ¹²¹ Walton et al, 1999. The application of in vitro data in the derivation of the acceptable daily intake of food additives. Food Chem Toxicol. 1999 Dec;37(12):1175-97. https://pubmed.ncbi.nlm.nih.gov/10654594/
- ¹²² Galli et al, 2008. Is the acceptable daily intake as presently used an axiom or a dogma? Toxicol Lett. 2008 Aug 15;180(2):93-9. https://pubmed.ncbi.nlm.nih.gov/18588960/
- ¹²³ Phillips et al, 2024. Improving the integration of epidemiological data into human health risk assessment: What risk assessors told us they want. Glob Epidemiol. 2024 Sep 28;8:100167. https://www.sciencedirect.com/science/article/pii/S2590113324000336
- ¹²⁴ Debras et al, 2022. Artificial sweeteners and cancer risk: Results from the NutriNet-Santé population-based cohort study. PLoS Med 19(3): e1003950. https://journals.plos.org/plosmedicine/article?id=10.1371/journal.pmed.1003950
- ¹²⁵ Debras et al, 2022. Artificial sweeteners and risk of cardiovascular diseases: results from the prospective NutriNet-Santé cohort BMJ 2022; 378 :e071204. https://www.bmj.com/content/378/bmj-2022-071204.full
- ¹²⁶ Debras et al, 2023. Artificial Sweeteners and Risk of Type 2 Diabetes in the Prospective NutriNet-Santé Cohort. Diabetes Care. 2023 Sep 1;46(9):1681-1690. https://pmc.ncbi.nlm.nih.gov/articles/PMC10465821/
- ¹²⁷ Chia et al, 2016. Chronic Low-Calorie Sweetener Use and Risk of Abdominal Obesity among Older Adults: A Cohort Study. PLoS One. 2016 Nov 23;11(11):e0167241. https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0167241#sec021
- ¹²⁸ Azad et al, 2020. Nonnutritive sweetener consumption during pregnancy, adiposity, and adipocyte differentiation in offspring: evidence from humans, mice, and cells. Int J Obes (Lond). 2020 Oct;44(10):2137-2148. https://www.nature.com/articles/s41366-020-0575-x
- ¹²⁹ Food and Agriculture Organization, 2025. State of Research on the Interactions between Food Additives, the Gut Microbiome and the Host. A Food Safety Perspective. Food Safety and Quality Series. https://openknowledge.fao.org/server/api/core/bitstreams/54e3c4a1-e95b-4365-b9ae-f99a75436106/content
- ¹³⁰ French Agency for Food, Environmental and Occupational Health & Safety, 2015. Évaluation
- des bénéfices et des risques nutritionnels des édulcorants intenses. Avis de l’Anses, Rapport d’expertise collective, Janvier 2015. https://www.anses.fr/fr/system/files/NUT2011sa0161Ra.pdf
- ¹³¹ Engel et al, 2018. Effect of high milk and sugar-sweetened and non-caloric soft drink intake on insulin sensitivity after 6 months in overweight and obese adults: a randomized controlled trial. Eur J Clin Nutr. 2018 Mar;72(3):358-366. https://pubmed.ncbi.nlm.nih.gov/29235560/
- ¹³² Chia et al, 2016. Chronic Low-Calorie Sweetener Use and Risk of Abdominal Obesity among Older Adults: A Cohort Study. PLoS One. 2016 Nov 23;11(11):e0167241. https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0167241#sec021
- ¹³³ French Agency for Food, Environmental and Occupational Health & Safety, 2015. Évaluation
- des bénéfices et des risques nutritionnels des édulcorants intenses. Avis de l’Anses, Rapport d’expertise collective, Janvier 2015. https://www.anses.fr/fr/system/files/NUT2011sa0161Ra.pdf
- ¹³⁴ Pepino, 2016. Metabolic effects of non-nutritive sweeteners. Physiol Behav. 2015 Dec 1;152(Pt B):450-5. doi: 10.1016/j.physbeh.2015.06.024. Epub 2015 Jun 19. https://pmc.ncbi.nlm.nih.gov/articles/PMC4661066/
- ¹³⁵ Rother et al, 2018. How Non-nutritive Sweeteners Influence Hormones and Health. Trends Endocrinol Metab. 2018 Jul;29(7):455-467. https://www.sciencedirect.com/science/article/abs/pii/S1043276018300936
- ¹³⁶ Regulation No 178/2002 of the European Parliament and of the Council of 28 January 2002. https://eur-lex.europa.eu/legal-content/EN/TXT/HTML/?uri=CELEX:02002R0178-20240701






Vous êtes hypocrite, pour quoi ne pas faire une petition contre le sucre qui est la cause numero 1 de developper un cancer (car ça cause l’obésité, etc.. etc…)
Bonjour et merci à Yuka de nous faire cette analyse poussée.
Je viens de regarder également ce que propose McDonald’s par exemple dans ces menus quand on achète un menu on a un coca on peut prendre de l’eau évidemment. On a également du coca sans sucre qui est noté B au nutri-score selon eux mais aucune mention d’aspartame alors qu’à priori selon le site de Coca-Cola ils en utilisent. Donc c’est quoi cette honte de mettre une note un nutri-score B.
Pour ma part je n’utilise pas le nutri-score mais plutôt la note de yucca qui est beaucoup plus détaillée.
De plus à l’heure actuelle le Coca-Cola classique est vendu plus cher 14 centime dû à la taxe sur les produits sucrés. Alors que le Coca-Cola sans sucre et moins cher donc tous les jeunes qui vont acheter des menus vont forcément prendre ce qu’il y a moins cher et manger de l’aspartame.
On en a pas fini avec cette édulcorant de synthès.
Merci pour cette enquête bien documentée et accessible – les médicaments aussi contiennent de plus en plus d’édulcorants, aspartam ou autre, et il devient compliqué de savoir quel est la bénéfice risque de certain traitements – il serait très utile d’informer également les consommateurs à ce sujet. qui pourrait le faire ? j’aimerais aussi en savoir plus sur les autres édulcorants, pas forcément si anodins que cela.
Bonsoir
Qu’elle est votre position sur l’Erythritol ? le Xylitol ? Le Yacon ?
Merci
Il y’a une pétition pour conserver l’aspartame ?
Votre article est complet, édifiant. Bravo pour ce travail rigoureux qui analyse et dénonce ce qui doit l’être. Depuis la création de Yuka, je reste absolument admiratif de votre pugnacité et de votre capacité à oeuvrer pour une bonne consommation alimentaire et pour la santé. 1000 bravos. Continuez !
L’aspartame a toujours été banni de l’alimentation de la famille, suspectant son rôle délétère
à qui et à quoi se fier de nos jours ?
risquer la vie de la population , de nos proches et tout ça pour faire du profit nous pouvons nous poser la question de savoir ou va l HUMANITE
On se fou de la santé de la population on préfère l argent .
C est une honte
NON A L ASPARTAM
Merci à Yuka, à La Ligue contre le cancer et à Foodwatch pour cette pétition, d’éveiller nos consciences, de nous informer et de nous alerter sur les risques alimentaires et leurs conséquences pour notre santé.
Il est important de savoir ce que l’on met dans notre assiette, de bien lire les étiquettes des produits achetés. Il faut se prendre en main, afin de faire le meilleur choix possible pour sa santé.
Il y a encore beaucoup de combats à mener dans le domaine de l’alimentation. Les lobbies de l’industrie agroalimentaire sont puissants mais rien ne vous oblige à acheter leurs produits ultra- transformés bourrés d’additifs, de colorants et d’arômes artificiels. Un vrai cocktail explosif.
Nous avons ce pouvoir là alors utilisons-le.
Les lobbies sont un véritable cancer pour nos sociétés. L’argent achète le pouvoir, cet article le démontre de façon flagrante.
nous sommes à la merci de toutes ces sociétés de l’agroalimentaire. Quoique nous faisons, nous sommes dans la nasse. Les enjeux financiers de cet empire régissent la planète et aucun gouvernement n’a les moyens de s’y opposer. A titre individuel, nous pouvons essayer – je dis bien essayer – de limiter les dégâts…
Quand je lis , l’argent, l’argent….., j’arrive à rester positif et je m’émerveille lorsque j’entends que la recherche avance et sauve des vies, qu’un homme retrouve la vue au bout de 20 ans, c’est tout ce qui compte, entendre le plus possible de bonnes nouvelles.
On doit se prendre en main le plus tôt possible, faire les bons choix, bien raisonner.
Scénario qui rappelle étrangement ce qui s’est passé avec les vaccins ARNm contre le covid…
Yuka c’est bonne éveil pour les gens, Aveugle pour leurs bien être aussi le bon alimentation zein et équilibrée. Je
commande .bon continuation pour les projets ………
Bonjour,
Qu’en est-il des chewing gum à base d’aspartame ? Pour calculer si on dépasse la dose journalière maximale recommandée, quelle est la quantité d’apartame dans un chewing gum ? La consommation de 2 à 3 chewing gum par jour est-elle nocive ? Merci
Le chewing-gum fait péter , car on avale de l’air. Mieux vaut le supprimer.
Le CIRC classe l’aspartame comme potentiellement cancérogène pour l’humain (Groupe 2B des Monographies du CIRC), évoquant des « indications limitées » de cancérogénicité chez l’humain, tout en confirmant l’innocuité de l’aspartame aux doses recommandées.
Le JECFA évalue les expositions moyennes et maximales à l’aspartame dans la population générale, et conclut que l’exposition à l’aspartame ne pose pas de problème de santé en respectant la DJA existante (40 mg/kg de poids corporel).
Vous tronquez les conclusions poit ne garder que les aspects anxiogène. C’est de la malhonnêteté intellectuelle.
Désolé, vous n’avez pas tout lu.
Le terme « indications limitées » ne signifie en aucun cas que les preuves seraient insuffisantes, comme on pourrait le comprendre dans le langage courant. Dans le cadre des évaluations du Centre international de recherche sur le cancer (CIRC), la définition est très précise : cela indique que des cas de cancers ont été observés de manière significative, mais qu’il n’est pas encore possible d’exclure totalement l’influence d’autres facteurs dans leur apparition. Il s’agit donc d’une classification importante, loin d’être négligeable.
Par ailleurs, l’avis du JECFA (entité dépendante de l’OMS) a été publié juste avant celui du CIRC et n’intègre pas le risque de cancer. Cet avis repose essentiellement sur l’étude très controversée de 1981 réalisé par l’industriel Ajinomoto, et écarte les résultats plus récents et solides de l’Institut Ramazzini ainsi que de l’INSERM. Cette position entre directement en contradiction avec les conclusions du CIRC. Comme mentionné dans cet article, plusieurs organismes ont d’ailleurs signalé un manque de transparence et des conflits d’intérêts au sein du JECFA lors de l’élaboration de son avis sur l’aspartame.
Nous demandons donc simplement que la dose journalière admissible (DJA) soit réévaluée en prenant en compte l’ensemble des données toxicologiques, y compris le risque cancérogène, ce qui n’a été fait ni par le JECFA, ni par l’EFSA. Le CIRC, pour sa part, n’a pas formulé de commentaire sur le risque aux doses actuellement utilisées, car cela ne relève pas de son champ de compétence.
J’espère ainsi avoir répondu à vos interrogations et vous avoir rassuré quant à la rigueur et à l’exhaustivité de notre analyse ✨
Zoé Kerlo, Toxicologue chez Yuka
Une fois de plus on constate que les gesticulations et les postures de nos soi-disant autorités de santé ne servent que des lobbies de l’agro-alimentaire et donc de l’argent.
Je crois qu’il devient illusoire de penser qu’il soit possible de manger sainement dans ce monde où quelques puissants font les lois et le règlements.
Non ce n’est pas encore tout à fait illusoire…Dans tous les cas :
– ne pas croire les industriels (qui ne nous veulent pas du bien mais uniquement notre pognon), ni leur pubs et ne pas consommer leurs salo..ries de produits transformés,
– do it your self,
– consommer bio et si possible des produits frais ou secs, bio et local,
– savoir que le seul « super pouvoir » que nous ayons dans ce monde cynique et cruellement marchand est notre capacité de consommer avec discernement et de manière discriminatoire (càd en éliminant au maximum ce qui peut être dangereux pour nous et nos descendants dans nos achats quotidiens).
Avec ça, les puissants peuvent toujours faire les lois et règlements, vous n’êtes ni obliger de les écouter, ni de les suivre.
À bon entendeur…
Cette enquête parle t’elle des médicaments pris quotidiennement contenant de l’aspartame ?
Article très intéressant et complet, qui se lit comme un roman policier. Quand toutes ces institutions qui lavent plus blanc que blanc seront-elles totalement indépendantes et sanctionnées pour laisser prise aux conflits d’intérêts ?
Les institutions ne seront jamais sanctionnées ni inquiétées et les industriels qu’elles défendent le seront, peut-être dans très longtemps et après des actions en justice…souvenez-vous de l’industrie du tabac ! Les industriels se foutent de votre life. Ce qu’ils veulent c’est votre pognon. Et pour cela ils vous tuent à petit feu car, il faut bien vivre ma ptite dame, vous diront-ils et de l’autre côté il y a aussi l’industrie pharmaceutique, vous savez celle qui tue à petit feu aussi mais avec des médicaments (médica…MENT s), qui soignent vos symptômes mais pas les causes des maladies…causes que l’homme s’ingénie à créer.
Nous consommons tous de
L’ Hexane ( pétrole) et rien n’apparaît sur les étiquettes de toutes l’alimentations.
Émission le mag de la santé, France 5 mercredi.
Je savais que se n’était pas bon je ne consomme jamais je me méfie de tout je sui très septique de toute façon tout et chimiques
Encore un énième scandale, si seulement c’était le dernier mais j’en doute !!!
J’ai lu entièrement votre enquête. Merci de m’avoir averti sur les effets de l’aspartame. J’ai signé la pétition. Bravo pour votre travail YUKA !
Bravo pour votre article très éclairant !
Merci pour toutes ces précisions sur l’aspartame. Soyons aux aguets car il y a du boulot …
Bonjour. Diabetiqua type 1, j’ai pris pendant des années de l »aspartam pour sucrer mes cafés et dans mes boissons. On me l »a présenté comme inoffensif par des diambetologues. Et puis….maux de ventre,soif intense besoin de plus en plus de boissons sucrees avec ce poison. Jusqu’au jour où j’ai lu une enquête. J’ai décidé d’arreter pile et j »ai ressenti comme des effets de manque. J »ai tenu bon et j’utile du miel bio pressé à froid. Ma glycemie est meilleure!!!
Inadmissible on ne peut plus faire confiance
Si bien sûr : ayez confiance en vous !-)
Bonjour à tout le monde.
Je signe cette pétition, car en réalité disons de cruellement : c’est une question de vie ou de mort.
On ne peut pas l’éviter mais il faut être vigilant. Depuis des années je prends de la STEVIA, j’ai du diabète type 2. Mais sans savoir ses défauts. Bien ou pas ? Aucun article complet là dessus.
Très bonne question, je regarderai si t’as eu une réponse…
Pour ma part, j’ai plutôt tendance à favoriser la fleur de Coco. Mais bien sûr je consomme de l’aspartame notamment dans tout ce qui est noté « sans sucre ». Qu’en est-il pour les chewing-gums et les medicaments « sans sucre » ?
Merci de nous ouvrir les yeux !
Curiosité et douter de tout ceci approuvé par nos chers législateurs, lobbyistes…
Retour au naturel, simple et fait maison. La nourriture est un des piliers basics de la santé
J’ai réussi à arrêter de fumer, j’ai réussi à arrêter de boire de l’alcool mais pour le sucre je n’arrive pas à décrocher .Choisir entre le sucre et l’aspartane c’est comme choisir entre la peste et le choléra
le sucre c’est largement « moins pire » il me semble (en quantités raisonnables, et selon l’état de santé diabète etc).
Merci pour cet éclairage
L’ aspartame ne m’a jamais inspiré. C’ est un produit chimique et comme tous les produits chimiques, ce n’ est pas un produit de consommation. J’ ai vu des gens en consommer depuis longtemps parce qu’ ils étaient trop gros et qu’ ils n’ arrivaient pas à se passer de sucre ou parce qu’ ils cherchaient une alternative aux boissons alcoolisées. Ce sont donc sur des personnes addictives et en surpoids sur lesquels se sont portées les essais cliniques. Aussi, les essais sur les rats me semble plus intéressant que ceux effectués sur les humains. Après, je pense que l’ on doit considérer l’ aspartame plus comme un pis aller pour personne diabétique ou en surpoids addict au sucre et qu’ en aucun cas on ne devrait en retrouver dans des aliments et des boissons. Ce produit ne devrait être délivré que sur ordonnance dans des cas bien précis de manière provisoire pour des diabétiques ou des obèses suivant une cure de désintoxication au sucre, ce dernier produit étant considéré également maintenant comme un produit à l’ origine de l’ augmentation des maladies cardio vasculaire.
Texte beaucoup trop long , mais interessant. Je n’ai jamais consommé cet ingrédient . Malheureusement il y a beaucoup d’autres produits inquiétants.
Tu crois ne l’avoir jamais consommer. J’en suis allergique et je peux t’assurer qu’il y est aussi dans + de 600 médicaments. Par exemple? tu le trouveS dans pratiquement tout les sirops contre la toux, les expectorant tel que le lysomucil etc etc Donc, même les personnes qui ne consomme aucuns sodas sans le savoir consomment de l’aspartame …..
Je ne consomme plus aucun sodas ni plats industriels et depuis 30 ans, je me soigne avec des médicaments homéopathiques (demandez-vous pourquoi l’homéopathie n’est plus remboursée depuis 2021…). Je pense donc échapper à cette cochonnerie d’aspartame. J’ai un ami qui en a consommer longtemps et qui est atteint d’alzheimer. Le seul réel pouvoir que nous ayons c’est notre pouvoir d’achat. Votez avec votre portefeuille ! Vous voulez mangez sainement ? Acheter des produits sain (pas bénis non plus, hein !-)
Quant on veut tuer son chien on dit qu’il a la rage!!
quel marché « volé » aux sucriers!!!!
que d’études ,quel acharnement
Heureusement que les spécialistes pétitionnaires font foie
Dénigrement dénué d’arguments des études scientifiques citées dans l’article. Appartenez-vous au lobby de l’aspartame ?
Merci pour ces importations ,maintenant je ferai 4 fois plus attention à la nourriture .
Merci pour ces importations ,maintenant je ferai 4 fois plus attention à la nourriture
Tu là dis 2 fois
donc ça fait 16 fois plus attention
Très intéressant… Un produit de plus à éviter : plastique, insecticide, engrais, sucre, métaux lourds ….
Le combat est rude
Déséspérant de constater qu’on nous empoisonne…plus grand choix pour être séléctif ds notre alimentation et un budget publicitaire pour bien influencer les consommateurs ..dorénavant je ne me fie qu’à YUKA
BRAVO ENCORE
MERCI
Dans votre très bon article vous ne signaler pas que le Japon n’a jamais autorisé l’aspartame c’est pourquoi ils ont mis au point le stévia qui est de loin le moins toxique des édulcorants
money money! industies alimentaires, labo pharmaceutiques tu sais plus ce que tu avales 🙂
le mieux prendre du traditionnel sans excès et se méfier toujours des nouveautés
grand merci à tous les lanceurs d’alertes qui nous informent ..
Jamais pris d Aspartame pour remplacer le sucre. Merci pour tout le développement sur l appartement. Très intéressant.
Bonjour, svp est-ce que l édulcorants est présent sur tous les yaourts et boissons?
Non il fait lire les petite lignes des ingrédients (ou utiliser Yuka). On peut même s habituer aux yaourts sans sucre comme au café noir dans sucre;-)
Les petits suisses nature sont très bons, j’ai entendu plusieurs fois qu’ils valent le Skyr.
Ne pas acheter le 0%, la marque Délisse est bien notée
Quand les industriels préfèrent gagner plus sans penser a protéger leurs propres descendants .. Car a l’heure actuelle, il y en a dans toute sorte de produits!
Ne vous en faites pas pour les descendants de ces empoisonneurs. Soit ils savent et évitent la consommation, soit ils s’en foute ou alors se paient des spécialistes. De toute façons, à partir du moment où une personne idolâtre l’argent, elle devient inconsciente. Et c’est fou le nombre d’inconscients dans notre monde…autant dans les « hautes sphères » que dans la masse silencieuse qui les subit !
Article trop long. On finit par se lasser. Certaines revues font des synthèses dans lesquelles on lit l’essentiel et on apprend 90% de la teneur de l’article.
Par ailleurs, haro sur l’aspartame : soit ! Mais il eut été plus intéressant pour nous consommateurs de faire un comparatif « sucre – aspartame ». Quel est le moins mauvais des deux ?
Je ne suis pas sûr que les lobbies du sucre aient été moins actifs que les lobbies de l’aspartame pour biaiser les résultats et « plomber » l’aspartame concurrent. Ils l’ont bien fait avec le gras
J’étais un consommateur d’aspartame pour compenser le sucre(conseils donnés par des professionnels de santé) J’ai donc mis un ou deux édulcorants dans mes cafés et thés quotidiens pendant de nombreuses années. Je pense que ce comportement est assez répandu. Ce serait pertinent de calculer le nombre d’édulcorants maximum à prendre par jour. J’ai réussi à les supprimer mais je suis encore addict au goût sucré (j’ai 75 ans)
Cher Denis est de un réel problème d’aimer le sucre ? Tant qu’il est consommé raisonnablement ? Tout supprimer n’est pas une bonne idée non plus selon moi. Je continuerai donc à manger mon carré de chocolat noir le soir ….
Cher Denis est de un réel problème d’aimer le sucre ? Tant qu’il est consommé raisonnablement ? Tout supprimer n’est pas une bonne idée non plus selon moi. Je continuerai donc à manger mon carré de chocolat noir le soir ….
Article super intéressant. C’est toujours une question d’argent peu importe la santé!
Laissons faire les vrais experts
quelle honte!! nous achetons de plus en plus de poison et,au prix fort,sur qui de nos jours pouvons nous compter?Et tout ça pour le fric..
Ne comptez que sur vous même. Vous savez que vous valez bien plus que leur argent.
D’apparence je féliciterai le travail de recherche biblio qui a été fait pour rédiger cet article de blog. Il manque cependant un esprit critique sur les analyses des articles qui sont mentionnés. Notamment sur les inférences qui sont faites sur les analyses statistiques. Il y a des généralisations qui sont faites alors que certaines études ne portent que sur un seul édulcorant – notamment Suez et al., 2014 qui n’étudient en réalité que la saccharine sur 7 volontaires et 7 jours (ce n’est qu’un exemple parmi tant d’autres). En statistiques, pour faire des inférences on évalue sur de grands effectifs, et de manière randomisée avec des contrôles actifs. Enfin, beaucoup confondent corrélation et causalité. Les risques de confusion (mode de vie, alimentation globale, activité physique, autres additifs ou contaminants, etc.) sont importants. Il faut des études longitudinales contrôlées, randomisées si possibles, ou des méta-analyses solides pour établir une causalité. Cette erreur est très répandue dans la communauté scientifique, et malheureusement, ce n’est pas parce qu’un article est publié dans une revue à H-index élevé (ce que vous appelez prestigieux) qu’il s’agit d’un bon article. C’est tout l’objet des formations d’éthique de la recherche qui deviennent maintenant obligatoires pour les nouveaux doctorants.
Merci pour ces précisions, j’ai lu des références plus rassurantes des sur des études qui ne semblent pas biaisées comme celles dénoncées dans l’article, qui comme vous le soulignez a tendance a insister sur des corrélations sans en montrer le lien de causalité. Je consomme régulièrement de manière non quotidienne des produits à base d’édulcorants, je surveille régulièrement « l’état de l’art » sur le sujet, et pour le moment, je ne trouve pas d’ensembles de méta études probantes contre ces derniers.
Tiens deux clones ou…clowns (?), dont l’un fait écho à l’autre ! Comme quoi les lobbys veillent au grain. Faciles à repérer car la stratégie de tout bon lobbyiste qui se respecte est toujours la même : semer le doute. À bon entendeur !
Quand un « produit » est autant controversé, on évite d’en consommer. Certes, ça ne fait pas avancer le schmilblick, mais un peu de bon sens ne fait pas de mal.
Vous savez, le bon sens, c’est comme le trou du ***, chacun à le sien 🙂 Appuyons nous plutôt sur la science.
Le fait est que vous avez besoin de la science pour démontrer qu’il est controversé. Et si vous ne faîtes pas de la science avec un minimum de bon sens et de méthodologie. Votre argument ne vaut rien. Laissez la parole aux scientifiques qui ont de l’éthique. CQFD.
Bonjour,
L’étude Suez et al de 2014 est citée car il s’agit de la première étude sur le sujet du microbiote, mais de très nombreuses autres études spécifiques à l’aspartame nous ont permis d’identifier un réel risque. En réalité, pour chaque risque mentionné dans cette enquête, nous nous sommes basés sur une importante quantité de données 📚 Cependant seules quelques études sont détaillées ici par souci de synthèse.
Ensuite concernant le lien de causalité, vous avez raison, il faut de nombreuses études solides pour correctement établir un risque pour la santé, selon la méthodologie du poids de la preuve. Pour être précis il faut 3 types de données : preuves sur l’humain, preuves sur l’animal et également des études in vitro permettant d’identifier un mécanisme d’action toxique cohérent. Il se trouve que pour plusieurs risques, notamment le risque de cancer, de nombreuses études pour chacun de ces points incriminent l’aspartame. Cela est expliqué dans le rapport de 471 pages du Centre international de recherche sur le cancer (source 70 de notre enquête).
Merci beaucoup pour votre commentaire, c’est très important de questionner la méthodologie de tout article. J’espère avoir répondu à vos questionnements.
Zoé Kerlo, toxicologue chez Yuka
Quid de la cyclamate ?
J’en prends depuis 1968
Avide de ce genre d’article, merci.
Les pouvoirs publics et le business souvent intimement liés sont aveugles et sourds lorsque pourtant nous parlons de santé publique. Nonobstant, s’agissant bien de la leur, CQFD.
Trop de passerelles et de points communs (l’idolâtrie de l’argent, le goût du secret, voire du mensonge, le cynisme, l’inconscience, la déshinibition extrême…) entre pouvoir et industrie…le premier se recyclant aisément chez le second pour son plus grand profit (ex. notre ex ministre, Castaner chez Shein…).
On peut éviter les aliments et les boissons contenant de l’aspartame. Ce qui m’inquiète le pus, c’est quand en lisant la formule certains médicaments (sirops, comprimés effervescents…) je découvre qu’ils en contiennent.
J’espère vraiment que ça va passer l’interdiction.
Étude complète et bien documentée, et surtout très facile à comprendre pour les non-scientifiques. Ce qui fait très peur, c’est de se rendre compte que l’argent arrive à corrompre de grands experts scientifiques.
L’argent corrompt tout et la plupart. Surtout depuis qu’il est redevenu la l’idole d’une majorité dans le monde par rapport à la spiritualité. Nous sombrons par son poids !
Ne consommons pas d’aspartame c’est peut-être la solution
Si les ventes diminuent en masse les industriels comprendront
Oui c’est exactement ça et c’est même le seul pouvoir que nous ayons quand on voit que voter ne sert plus à grand chose, en tout cas pas à faire advenir les changements attendus.
Bonjour
J ai écrit directement à Yuka mais à tous ceux qui vont dans leur sens que répondez vous au fléau qu’est l’obésité ? Alors bien sûr que l’on peut boire de l’eau et autre tisane et thé sans sucre mais quand on en peu plus je pense qu’un soda zéro vaut mieux qu’un soda normal qui contient un nombre indécent de morceaux de sucre. Et si on ne boit plus de soda zéro qu’elle est l’alternative svp ?
L’alternative c’est de ne plus consommer ces merdes!
Bonjour, bien sûr nous ne conseillons pas non plus la consommation régulière de sodas sucrés, dont le lien avec l’obésité est largement démontré. Cette enquête met simplement en évidence que l’aspartame n’est pas la solution miracle : à long terme, il pourrait lui aussi favoriser une prise de poids. En réalité, la seule véritable alternative reste de limiter la consommation de sodas, quels qu’ils soient, à un usage occasionnel et de se déshabituer progressivement du goût sucré.
Bon courage ✨
Zoé Kerlo, toxicologue chez Yuka
Kéfir ou kombucha maison…do it your self !
Je suis foutue alors. Cela fait au moins 25 ans que je machouille du chewing gum à l’aspartame après avoir arrêté de fumer, habitude dont il va être difficile de se débarrasser et puis, après votre article alarmiste, je me demande si ça en vaut la peine.
Merci Julie pour les informations sur l’aspartame mais hélas, nous sommes en 2025,et malgré les avertissements que je connais depuis longtemps sûr cet additif,rien n’est fait pour le supprimer et ça me mets en colère contre les industriels qui s’en foutent et s’en mettent pleins les poches 😚
C est le point faible.
Oui il faut beaucoup de bon sens pour éviter ces nouveautés vendues à grands renfort de pub. Étant sportif, j’aime et je consomme pas mal de sucre. Lors de la sortie de l’aspartame en France au siècle dernier, je l’ai goûté pour savoir ce que c’était mais je suis resté au sucre car ce produit de synthèse capable de remplacer X morceaux de sucre m’avait paru suspect voire proche du tour de passe passe. Et c’est bien celui de vouloir « vendre des vessies pour des lanternes ». Peu d’industriels sont honnêtes, il faut le savoir.
Bravo pour cet excellent article ! Pourriez-vous nous conseiller une alternative à l’aspartame, nous qui, pour des raisons médicales, ne pouvons pas consommer du sucre et qui sommes « obligés » d’utiliser de l’aspartame pour notre nourriture quotidienne ? D’avance, un grand merci.
Bonjour Thi,
J’ai du mal a comprendre le mot « obligé » d’utiliser de l’aspartame. L’aspartame est présent dans des produits spécifiques, boisons, dessert… A quel moment le sucre ou l’aspartame sont obligatoires ?
Je pense qu’on peut se passer des deux… Mais je me trompe surement…
Si on ne peut pas s’en passer on peut en tout cas, avec un effort de volonté, réduire le sucre, ne pas en consommer en dehors des repas et se passer complètement de l’édulcorant de synthèse.
Le Steva peut-être…
Bonjour,
Malheureusement la seule vraie solution pour tout le monde serait de se déshabituer au goût sucré. Pour les consommations occasionnelles, il faut se tourner vers votre médecin pour trouver la solution la plus adaptée à votre cas. Car en effet, pour les personnes avec des pathologies les obligeants à fortement limiter la consommation de sucre, comme les personnes souffrant de diabète, il est possible que les édulcorants soient à privilégier dans certains cas.
Bon courage à vous 💪
Zoé Kerlo, Toxicologue chez Yuka
Article très intéressant et constructif avec arguments et contre-arguments. Le constat est une fois de plus navrant : nous sommes dans une société gérée uniquement par l’appât du gain et du pouvoir, où l’on prend vraiment les gens pour des demeurés ! La nourriture totalement saine existe-t-elle encore ? Je n’y crois plus 😔.
« Saine » je ne pense pas, nous avons déjà trop pollué notre planète qui elle, nous survivra.
Cela fait tres lomgtemp lomgtemp que je connaissais ce problème
Merci de le faire lire au gens
Ce serait formidable si vous
Faite de même pour les problème
Des microhondes
Bonjour Josette, vous êtes une grande experte scientifique semble t’il. Pour le micro-onde, instruisez-vous en lisant ceci: https://htc-sante.com/dangers-micro-ondes. Même l’OMS est d’accord pour dire que le micro-onde ne procure aucun problème pour la santé. Et même mieux, plus le temps de cuisson est court et meilleur est la qualité du produit cuit. La cuisson par micro-ondes, c’est pas de la pétrochimie. On fait chauffer l’eau qui se trouve dans les aliments ce qui permet de chauffer l’ensemble du produit tout en conservant les vitamines et ses qualités. Déjà que vous ne savez pas écrire correctement le français (y’a pas de h à micro-onde alors pour la physique, … C’est comme les écolos pour le nucléaire, c’est l’énergie la plus propre, c’est de la vapeur d’eau qui sort des cheminées ou plutôt aéroréfrigérants. Alors les fake news, ça y va ! Allez, je ne vous en veux pas, bien à vous.
J’oubliais, c’est un n à lomgtemps, donc ça s’écrit longtemps comme temps long.
Ben…encore heureux que vous ne lui en veuillez pas ! Et à par ça que faites vous des déchets nucléaires ? Vous les enfouissez…à Bure, parce que ce n’est pas dans votre coin coin et que vous croyez tout ce que raconte des ingénieurs qui seront décédés depuis longtemps quand il y aura un problème de pollution de la nappe phréatique ?
Bien sur, Jean-Michel, je m’excuse d’avance pour les fôtes d’orthographe intentionnelles ;-/
bravo pour votre article bien documenté, accessible à lire et alertant !
top, ceux qui trouve ça trop long, lachez vos séries, et lisez ce qui peut tre bon pour votre santé…
Bravo pour cette synthèse parfaitement et chronologiquement bien étayée des différents éléments de controverse !
Elle apporte tous les éclaircissements sur la mise sur le marché de cette substance très controversée et les risques liés à sa consommation.
A diffuser le plus largement possible
Merci pour vos informations très documentées. Cela confirme qu’il n’est plus possible de faire confiance aux organismes de contrôle officiels. Même combat avec les pesticides, engrais, etc
Merci pour ce compte rendu détaillé et intéressant de la situation dramatique dans laquelle le consommateur se trouve!
Il est plus que temps d’agir…
Bravo
Merci beaucoup pour ces informations très détaillées. Je fais suivre immédiatement à mes enfants !
Et qu’en est-il du sucralose au pouvoir encore plus sucrant – 5 à 600 fois celui du sucre- et que l’on retrouve de plus en plus dans l’alimentation, notamment compléments alimentaires et produits vegan ?
instructif que de choses caché merci pour l »article
Merci á vous.
Du coup, Je vais boire un verre d’eau, de source !! Enfin peut etre …😅
…sans PFAS !-)
Merci, Merci encore pour vos informations, malheureusement je crois que nous sommes impuissant dans se monde de crapules, mais il faut quand même continuer de se battre pour sauver nos enfants
Votre enquête est claire, nette et précise. J’adhère !
Bonjour, félicitations pour cette énorme travail très complet et très informatif.
Cela gagne véritablement être partagé avec son entourage.
PS : le lien de la source numéro 11 est cassé
Félicitations pour cet article extrêmement fouillé et détaillé sur l’aspartame, c’est un immense travail de recherche et je signe votre pétition.
Merci pour votre engagement.
Un énième dysfonctionnement de notre société où le profil est toujours prioritaire sur l’humain…des scandales alimentaires il n’y a beaucoup t sans une volonté ferme et courageuse du politique rien ne changera hélas…un scandale en chasse un autre…l’humain est un être versatile…il oublie vite…nous sommes aussi responsables nous CON-SOMMATEUR…car il suffirait de ne plus acheter ces produits toxiques pour notre santé pour que les industriels ne les produisent plus…nous avons le pouvoir mais nous ne nous en saisissons pas…c’est dommage…sommes nous des moutons 🐑, incapables de se defendre er qui laissons les lobbies jouer avec nos vies
Le pouvoir pour le monde politico industrialo médiaticorrect c’est votre argent et il faut essayer de leur en donner le moins possible. C’est notre responsabilité.
Bonjour,
Merci pour cet article.
Je fais partie de la génération qui a porté et profité de toutes ces innovations technologiques. Je travaille dans l’alimentaire et j’ai vu tout au long de ma vie s’éloigner le lien qui existe normalement entre la nature et l’alimentation. Il y a aujourd’hui plus de pétrole que de soleil dans nos aliments. L’aspartam fait partie de cela. La technique a été (et continue d’être) la réponse apportée à la faiblesse de l’homme. Nous avons externalisé tous nos problèmes, nos faiblesses, d’abord par l’outil puis ensuite la technique. Le capitalisme a, comme toujours, intégré en son sein nos faiblesses pour développer des réponses qui produisent de larges profits. Il ne faut pas se leurrer, quelle que soit la « sincérité éthique » de tous les marchands, ces produits « sans sucre » contiennent autant sinon plus de richesse que les « avec sucre », mais aussi bien de maux. La sagesse et la notion de Bon Sens et les idées associées développées par Descartes en 1637 dans son « Discours de la méthode » me semblent bien actuelles.
Dans l’industrie de la restauration, on ne cesse de vendre aux professionnels des produits qui garantissent une meilleure productivité, une plus grande facilité de mise en œuvre, un bénéfice accru. Malheureusement, la restauration commerciale échappe à la transparence. Il n’y a aucun affichage dans les pâtisseries concernant la composition des gâteaux proposés.
Seule la restauration collective a su se réformer en obligeant une grande transparence. Merci pour nos enfants ! Et un peu d’espoir dans cette marche forcée qui, vous semblez le dire, n’est pas prête de s’arrêter, mais que vous nous aidez à ralentir grandement.
Bonjour, et merci pour cette article.
J’ai du mal à me passer du gout du sucre dans le thé et dans le café, et j’utilise du SUCREDULCOR , un édulcorant à la saccharine. Ce produit est il moins nocif que l’ASPARTAM?
Et encore plus grave il y en a même dans les médicaments !
Merci pour cet article cela fait longtemps que je n’achète rien avec des édulcorants. Lorsque je fais un dessert je mets le moitié voire le tiers de sucre de canne bio
Je ne signe pas cette pétition parce que je suis certain que l’industrie sucrière est bien plus pénalisée par la mise sur le marché de tout les édulcorants de synthèse que la santé de ceux qui les consomment.
Comment peut-on dire que ces édulcorants favorisent le diabète de type 2 ? J’ai moi même gueri de ce diabète, après avoir été traité pendant 20 ans, sans résultats, en réduisant les sucres rafinés consommés et remplacés par l’Aspartame et maintenant par le sucralose.
Je ne poserais qu’une seule question : Citez moi 1 seule personne malade à cause de l’Aspartame et comparez au nombre des malades connus ou inconnus à cause du sucre rafiné.
Bonjour, bravo pour votre parcours !
Chez les personnes souffrant de diabète, le recours aux édulcorants peut effectivement parfois représenter la meilleure option, car dans leur cas, le sucre est directement toxique pour le métabolisme.
En revanche, dans la population générale, les résultats scientifiques sont plus préoccupants. Sur le long terme, l’aspartame perturberait le métabolisme du sucre en interagissant avec les récepteurs du goût sucré. Cette interaction favorise progressivement une résistance à l’insuline et augmente le risque de développer un diabète de type 2. C’est en tout cas les conclusions de nombreuses équipes de recherches et de l’Organisation mondiale de la santé (OMS).
J’espère avoir répondu à votre questionnement ✨
Zoé Kerlo, toxicologue chez Yuka
merci pour cet article documenté.
Que penser du corps médical qui a conseillé à mon petit-fils de 17 ans diabétique (depuis ses 8ans) de boire du Cocacola light lorsqu’il se sent en manque de sucre pour éviter le malaise. Les lobbies Cocacola et aspartame ont semble-il gagné jusqu’aux services de diabétologie…
Merci de répondre aussi svp au questionnement sur la Steva pour remplacer l’aspartame pour les diabétiques dans leur consommation courante pour remplacer le sucre
Bonjour Marie-José, si votre petit fils est diabétique, je peux vous assurer que ce n’est pas à cause des édulcorants de synthse mais des sucres rafinés comme les confiseries, le pain blanc, le riz blanc, les pattes blanches, les pommes de terre etc.. Il y a des sucres rafinés cachés partout. Pour votre petit fils, je pense qu’il est atteint d’un diabète de type 1 qui est vraiment une maladie inguérissable du au mauvais fonctionnement du pancréas.
Bonjour du sucre raffiné caché dans le riz , le pain et les pommes de terre ? Une explication, merci
Bonjour Julie, Merci pour ces informations très importantes pour notre santé, à nous de rester prudents 👍
Cela fait plus de 20 ans que j’évite tout ce qui contient de l’aspartame. Je note qu’on parle de l’alimentation mais de nombreux médicaments en contiennent et là difficile de l’éviter. J’espère que les médicaments seront egalement concernés s’il y avait retrait de l’aspartame.
Dans le doute, je vais désormais m’abstenir d’en consommer. Cependant, pas d’accord sur l’absence de bénéfice sur le poids, chez moi le passage au soda Light a fait une énorme différence. Cela dépend de chacun.
Très intéressant mais exposé exagérément long donc fastidieux
C’est excellent de lire, beaucoup moins de fautes d’orthographe
Très intéressant merci
Merci pour votre travail d information
Merci pour cette enquête très documentée par des sources bien établies , mais une synthèse raccourcie serait bien venue pour éviter une lecture trop lassante .
voici le résumé de ChatGPT (j’ai fait aussi avec Mistral, mais c’était moins bien):
https://chatgpt.com/s/t_68c9322be03481918ee497741f2531ff
Merci pour cet article très complet. Le sucre ou son édulcorant font parti d’une grande partie de l’alimentation transformée ou ultra transformée. Il n’y a pas une sauce tomate sans sucre ajoutée, pas une boîte de petits pois sans sucre ajouté etc… Utilisons le sucre, le vrai à bon escient et avec modération et peut-être que notre santé s’en trouvera améliorée. Apprenons à manger moins sucré au quotidien, à modérer nos quantités de sucre . Je n’achète plus de petits pois en conserve et je ne sucre pas mes yaourts, mon café, mon thé, le vrai goût n’en est que meilleur ….Mais je fais quand même, de temps en temps, des gâteaux pour le plaisir de mes enfants.
Merci pour cet article très intéressant.
MERCI BEAUCOUP pour cet éclairage précis ! Si je puis me permettre, pourriez-vous faire la même chose pour la Stevia ?
Encore merci.
Se focaliser sur l’aspartame alors que 30 % des français se disent fumeur et qu’on a encore de la pub pour des offres spéciales » salon du vin » tous les 4 mois…
Alors certes l’aspartame a montré un risque dans l’étude nutrinet mais faut relativiser le risque est de [HR] = 1.13 [95% CI 1.03 à 1.25] soit 1.13x plus qu’une personne lambda ( sans exclure que potentiellement c’est juste 1.03x +) … Sachant que la même cohorte montre un effet protecteur de consommation des fruits et légumes sur le risque de cancer…
En clair, aspartame vaut peut être pas mieux que le sucre mais dans une alimentation équilibrée et variées avec une pratique de sport pour éviter le surpoids/obésité et en modérant sa consommation d’alcool et ne pas fumer, vous faites le meilleur pour votre corps…
Prenez vous pas la tête ! Devenez pas parano non plus … On sait bien que les produits ultra transformé c’est pas terribles mais l’alimentation plaisir est tout aussi important
Quelle est le plaisir à consommer un produit dont la dangerosité est prouvée et qui donne un sale goût à l’alimentation?
Tout à fait d’accord Pierre, je ne connais pas une seule personne reconnue pour être malade à cause des édulcorants de synthèse par contre j’en connais énormément qui sont malades à cause des sucres raffinés. J’ai été diabétique de type 2 pendant 20 ans à prendre toutes sortes d’anti-diabétiques oraux jusqu’au jour ou j’ai pris les choses en main et cherché les aliments à indice glycémique faible, remplacé tout les sucres raffinés par de l’aspartame d’abord puis par le sucralose maintenant.
J’ai perdu, sans effort et en pleine forme, 38 kg en 9 mois et je ne suis plus diabétique depuis 15 ans.
VIVE le sucre raffiné
Ah non Robert ! Vive le sucre de canne bio consommé avec modération 😉
J’ai 78 ans, je ne bois que de l’eau, (pas d’alcool, pas de sodas) je ne fume pas, je mets de temps en temps de l’aspartame dans mon café (1 pilule) ou dans mon yaourt nature bio. Je ne vois pas l’intérêt d’interdire l’aspartame, il faut arrêter de prendre les gens pour des mineurs et avoir peur de tout. Le vrai problème est une question d’équilibre et de variété dans l’alimentation. Et dans ce domaine vous faites le job et j’apprécie, mais de grâce arrêtez le « bashing »……..
… et je ne pas l’intérêt pour vous de prendre de l’aspartam …
Quel est l’intérêt de mettre de l’aspartame dans votre yahourt si vous savez que c’est nocif? Une cuillère de sucre de canne non raffiné, c’est tellement meilleur!
BIEN DIT !!
Existe-t-il des alternatives inoffensives au sucre et à l’aspartame ? Sur Yuka, des additifs comme l’acésulfame-K (E950) ou le sucralose (E955) sont aussi présentés comme à risques, avec le même argumentaire que celui contre l’aspartame, mais ils ne font pourtant pas l’objet d’une pétition demandant leur interdiction. Si les industriels se reportent sur ces produits, l’effet sera donc le même pour les consommateurs ! Difficile de comprendre votre démarche dans ces conditions…
la STEVIA est elle bonne en remplacement ??
Il faut comprendre, et c’est précisé dans l’article, que tout ce qui est sucré sur la langue genere à minima des problèmes de résistance à l’insuline, sans parler du reste. IL FAUT ARRÊTER DE CHERCHER LE SUCRE PARTOUT. POINT. contentez vous des fruits, qui apportent bien d’autres choses que le fructose. Mais en quantité limité malgré tout.
Malheureusement la seule vraie solution serait de se déshabituer au goût sucré et à limiter la consommation de produits sucrés ou contenant des édulcorants à risque à une consommation occasionnelle. Car d’autres édulcorants, notamment ceux que vous mentionnez, comportent eux aussi des risques pour la santé.
L’aspartame reste toutefois un cas particulier : il est le seul édulcorant à avoir été classé comme « cancérogène possible » par le Centre international de recherche sur le cancer, et le seul additif dont l’autorisation a été entachée d’un historique aussi marqué de conflits d’intérêts.
J’espère avoir répondu à votre interrogation 🙂
Zoé Kerlo, Toxicologue chez Yuka
Merci Zoé pour l’article, vos réponses et précisions.
Merci pour le sérieux de votre article, cela peut nous apporter un point de vigilance sur ce que nous consommons et boycotter tous ces produits autant que possible.
Quid du stevia dans nos assiettes, verres et autres …?
Une synthèse aurait été la bienvenue.
Beaucoup de paragraphes redondants.
Chatgpt est votre ami, demandez-lui! 😅
Je ne pense pas que Chatgpt soit votre ami sinon vous avez de drôles d’amis. En tout cas ce n’est et ce ne sera pas le mien !
Merci beaucoup Julie et Zoé pour cette lecture très intéressante 🍀🌞